题目内容
【题目】能正确反映对应变化关系的图像是
A. 向一定量的稀硫酸中滴加氢氧化钠溶液至过量
向一定量的稀硫酸中滴加氢氧化钠溶液至过量
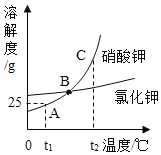
B.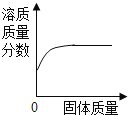 一定温度下,向不饱和硝酸钾溶液中不断加入硝酸钾固体,充分搅拌
一定温度下,向不饱和硝酸钾溶液中不断加入硝酸钾固体,充分搅拌
C. 将等质量的铁、锌两块金属分别与溶质质量分数相同且足量的稀硫酸反应
将等质量的铁、锌两块金属分别与溶质质量分数相同且足量的稀硫酸反应
D.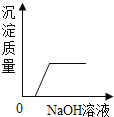 向FeCl3和HCl的混合溶液中滴加足量的NaOH溶液
向FeCl3和HCl的混合溶液中滴加足量的NaOH溶液
【答案】BD
【解析】
A.向一定量的稀硫酸中滴加氢氧化钠溶液至过量,pH值应从小于7开始,两者恰好完全反应时,pH=7,过量时,pH>7,故不对应;
B. 一定温度下,向不饱和硝酸钾溶液中不断加入硝酸钾固体,充分搅拌,开始硝酸钾溶解,饱和后,硝酸钾不会溶解,溶质质量分数先变大,变化后不变,对应;
C.将等质量的铁、锌两块金属分别与溶质质量分数相同且足量的稀硫酸反应,因为锌比铁活泼,反应时间应短些,等质量的两种金属铁产生氢气多,故不对应。
D.向FeCl3和HCl的混合溶液中滴加足量的NaOH溶液,开始氢氧化钠和盐酸反应不会生成沉淀,后来氢氧化钠和氯化铁反应生成氢氧化铁红褐色沉淀,对应。
故选BD。

 名校课堂系列答案
名校课堂系列答案【题目】兴趣小组在做完盐的性质实验后,发现一瓶碳酸钠固体可能混入了氯化钠、硫酸钠中的一种或两种。为此,他们取少量该样品于试管中,加入足量的水,溶解后进行了下列探究。
(实验验证)
实验步骤 | 现象 | 结论、分析及化学方程式 |
(1)滴入过量的稀硝酸,再滴入过量的硝酸钡溶液。 | 有气泡产生,____ | 说明该固体中没有硫酸钠。 |
(2)再继续滴入几滴硝酸银溶液。 | 有白色沉淀生成 | 说明该固体中______。实验结束所得溶液中一定含有的阳离子是______。 |
(实验反思)
(1)步骤(1)中先加入过量的稀硝酸的目的是______,写出该反应的化学方程式_______。
(2)步骤(1)中为什么不用稀盐酸______。
(3)写出步骤(2)的方程式_______。