题目内容
【题目】 “嫦娥三号”飞船的成功发射是我国航天事业的又一里程碑。金属过氧化物等可作宇宙飞船或潜水艇中的氧气再生剂,如:过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气和碳酸钠。为了验证该反应中氧气的产生,某兴趣小组的同学设计了如右图所示的实验。
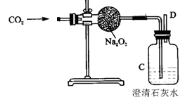
(1)为了确定CO2跟Na2O2反应产生的气体是氧气,最后还要采用的验证实验操作是:在D导管处放置一根______________________。
(2)_________________(填“现象”)说明二氧化碳已被过氧化钠完全吸收。
(3)若每人每天产生的二氧化碳的质量为2.2千克,若用过氧化钠将这些二氧化碳全部吸收,则理论上可产生氧气多少千克?(写出计算过程)
【答案】(1)带火星的木条;(2)C中的澄清石灰水不变浑浊;(3)0.8g
【解析】
试题分析:(1)为了确定CO2跟Na2O2反应产生的气体是氧气,最后还要采用的验证实验操作是:在D导管处放置一根带火星的木条,说明生成的气体为氧气;(2)C中的澄清石灰水不变浑浊说明二氧化碳已被过氧化钠完全吸收;(3)设每人每天产生的二氧化碳的质量为2.2千克,若用过氧化钠将这些二氧化碳全部吸收,则理论上可产生氧气X
2Na2O2 + 2CO2===2 Na2CO3 + O2
88 32
2.2kg x
88:32=2.2kg : x
X=0.8kg
答:理论产生氧气为0.8kg

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目