题目内容
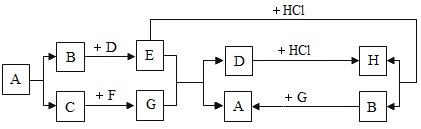
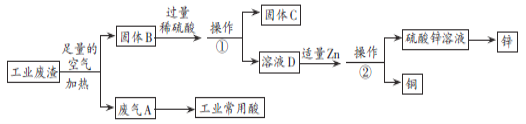
【题目】含硫的物质在实验室或工业生产过程中可出现下列图示的转化:
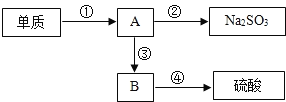
(1)实验室中,单质硫是_____色固体,点燃少量单质硫于充满氧气的集气瓶中燃烧,产生漂亮的蓝紫色火焰,生成物质A.
(2)A是工业排放物中一种主要的空气污染物,也是酸雨形成的主因之一.根据你学过的知识可将A转化成Na2SO3,你提供的试剂是________溶液.
(3)在硫酸工业中,将A在一定条件下与空气中的物质反应得到B,B与水结合得到硫酸.B与A的组成元素相同,B中硫元素与硫酸中硫元素化合价相同,写出A转化成B的化学方程式:___________________.实验室测定,B与水结合时温度升高,则反应④为_____反应(选填“吸热”或“放热”).
(4)上述物质转化过程中,属于化合反应的是______(填序号).
(5)若回收工业排放物A 32吨,理论上可生产硫酸_____吨.
【答案】黄 氢氧化钠 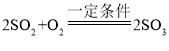 放热 ①③④ 49
放热 ①③④ 49
【解析】
(1)单质硫是黄色的固体,故填:黄;
(2)硫与氧气反应生成二氧化硫,二氧化硫能与氢氧化钠溶液反应生成亚硫酸钠和水,故填:氢氧化钠;
(3)二氧化硫能与氧气反应生成三氧化硫,三氧化硫能与水反应生成硫酸,B与水反应温度升高说明该反应是放热反应,故填: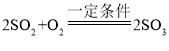 ,放热;
,放热;
(4)反应①是硫与氧气反应生成二氧化硫属于化合反应,反应②是二氧化硫与氢氧化钠生成亚硫酸钠和水的反应,不属于基本反应类型,反应③是二氧化硫与氧气生成三氧化硫的反应,属于化合反应,反应④是三氧化硫与水生成硫酸的反应,属于化合反应,故填:①③④;
(5)设生成硫酸的质量为x
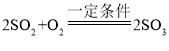 ,SO3+H2O=H2SO4,根据两个反应的关系,得出SO2和H2SO4的关系:
,SO3+H2O=H2SO4,根据两个反应的关系,得出SO2和H2SO4的关系:

![]()
x=49t
答:理论上可生成硫酸49吨。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】有一包白色粉末样品,其中含有碳酸钠、氢氧化钠、碳酸钙、生石灰、氯化钠、硫酸铜六种物质中的四种。化学兴趣小组为确定其组成设计并进行如下实验。
实验一:甲组同学进行定性探究
实验操作 | 实验现象 | 实验结论及分析 |
(1)取少量该样品于烧杯中,加入足量的水溶解、过滤 | 粉末部分溶解,得到白色滤渣和无色滤液 | 原样品中一定不含_____; |
(2)向滤液中滴加无色酚酞试液 | 溶液变红 | 滤液中存在_____性物质(填“酸”、“中”或“碱”) |
(3)向(2)中滴加足量稀盐酸 | _____ | 原样品中一定含有碳酸钠 |
实验二:乙组同学进行定量探究(如图)
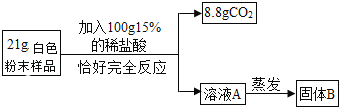
实验测得固体B中含15g氯元素,综合甲、乙两组同学的实验进行分析。
(1)乙组实验中一定发生的化学反应有碳酸钠与稀盐酸的反应和_____(用化学方程式表示)。
(2)该未知粉末的组成可能是_____。