题目内容
【题目】科学严谨的态度、安全规范的操作是成功进行化学实验的保障.
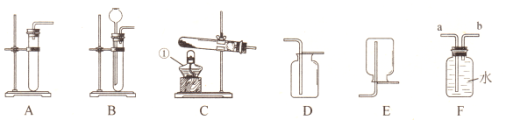
(1)化学实验安全第一,下列实验要特别注意安全的是________(填序号).
A.取用大理石 B.称量粗盐 C.稀释浓硫酸 D.研碎胆矾
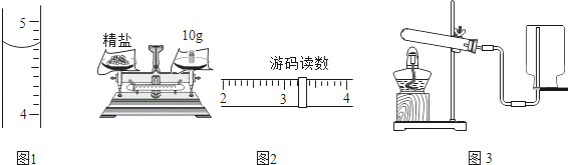
(2)根据图1和图2,读出液体的体积为________mL,精盐的质量是________g.
(3)实验室用图3所示的装置制取和收集某种气体,由装置可推知该气体的物理性质是________ , 制取气体的反应一定是________(填序号).
A.不需要加热 B.需要催化剂 C.制取氧气的反应 D.反应物都是固体
【答案】C4.713.2密度比空气小D
【解析】
(1)如果水加入浓硫酸时,水的密度小于浓硫酸的密度,在浓硫酸的上面,浓硫酸溶解放出大热量,使水沸腾,液体就会喷出伤人,因此,稀释浓硫酸时,一定要把浓硫酸慢慢倒入水中,并用玻璃棒不断搅拌,使产生的热量及时散发;
(2)量筒读数时,视线要与量筒内凹液面的最低处保持水平,读数为:4.7ml;药品的质量为托盘上砝码的质量与横梁上游码质量之和,精盐的质量是13.2g;
(3)用该装置来制取气体,说明反应物是固体加热制取气体,但不能说明一定使用了催化剂;用向下排空气法来收集,说明该气体的密度比空气小,不会是氧气。

 阅读快车系列答案
阅读快车系列答案【题目】在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】甲认为黑色颗粒是____,白色物质可能是(1)Na2O(2)碳酸钠
(3)___________________乙同学认为白色物质可能是氢氧化钠。甲同学立刻认为乙同学的猜想是错误的,其理由是_______________________________。
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠: Na2O+H2O == 2NaOH
【实验探究】甲同学对白色物质进行实验探究。
实验方案 | 实验操作 | 实验现象 | 结论 |
方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | _______ | 白色物质 为氧化钠。 |
方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | _______ | 白色物质 是碳酸钠。 |
②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | _______ |
【反思评价】丙同学认为方案1得到的结论不正确,其理由是_____________________。
【得出结论】钠在二氧化碳中燃烧的化学方程式为____________________________。由钠在二氧化碳中燃烧的实验还能得出什么结论?_________________(任意写一个)