题目内容
【题目】某碳酸钠样品中含有少量的氯化钠,现与测定样品中碳酸钠的含量,取该碳酸钠样品11.0g,加入稀盐酸100.0g(样品在的碳酸钠与稀盐酸恰好完全反应),反应后经称量,溶液的质量为106.6g.计算:
(1)碳酸钠样品中碳酸钠的质量分数.
(2)反应后溶液中溶质的质量分数.
【答案】(1)96.4%(2)11.4%
【解析】
根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳和对应的化学方程式求算碳酸钙和HCl的质量,进而求算对应的质量分数。
解:根据质量守恒定律可得,生成的二氧化碳的质量为11g+100g-106.6g=4.4g
设参加反应的碳酸钠的质量为x,生成的氯化钠的质量为y
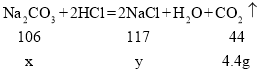
![]() =
=![]() =
=![]()
x=10.6g
y=11.7g
碳酸钠样品中碳酸钠的质量分数为![]() ×100%≈96.4%.
×100%≈96.4%.
反应后溶液中溶质的质量分数为![]() ×100%≈11.4%
×100%≈11.4%
答:(1)碳酸钠样品中碳酸钠的质量分数约为96.4%.
(2)反应后溶液中溶质的质量分数约为11.4%.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
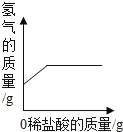
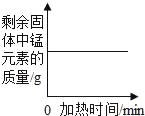
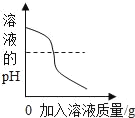
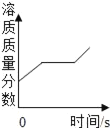
【题目】下表所述各实验过程中某些量之间的变化关系,其中正确的是( )
① | ② | ③ | ④ |
向一定量铁粉中滴加稀盐酸 | 加热一定量高锰酸钾固体 | 向稀盐酸中滴加过量的氢氧化钠溶液 | 将硝酸钾不饱和溶液恒温蒸发水分,直至有晶体析出 |
|
|
|
|
A. 只有①B. 只有②C. ①、②、④D. ②、③、④