题目内容
(1)化学是在分子原子层次上研究物质的科学,如图, A-D是四种粒子的结构示意图,请回答:
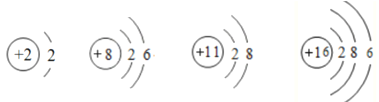
A B C D
在 A-D中,化学性质相似的原子是____;位于同一周期的元素是 ___;(以上两空均填字母);具有相对稳定结构的粒子是 ______ (填化学符号)。
(2)人类生产、生活离不开化学。
①厨房里可以用_来除去水壶中的水垢[水垢的主要成分是CaCO3和Mg( OH)2]。
②能用洗洁精除去餐具上的油污,是因为洗洁精对油污具有__作用。
③吃完学校美味的自助餐,赵子曦同学拿着还没开盖的可乐,跑回教室,打开瓶盖后,汽水喷涌而出,请用化学方程式解释其原因: ______。
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案某食用碱的主要成分是Na2CO3,其中含有少量的NaCl,小明同学为测定该食用碱中Na2CO3的质量分数,他进行了以下实验,取40 g食用碱,加水配成400g的溶液,把溶液平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
实验一 | 实验二 | 实验三 | 实验四 | |
食用碱溶液的质量 | 100g | 100g | 100g | 100g |
加入CaCl2溶液的质量 | 20g | 40g | 60g | 80g |
生成沉淀的质量 | 2.5g | 5g | m | 8g |
请分析表中数据并计算回答。
(1)m=________;
(2)40 g该食用碱配成的溶液与足量CaCl2溶液反应,最多生成沉淀质量为多少;
(3)该食用碱中Na2CO3的质量分数是?(写出计算过程,答案精确到0.1%)
(4)请根据实验四的数据画图并标上合适的坐标。

下列选用的除杂试剂和实验操作都正确的是(括号内为杂质)
选项 | 物质 | 除杂选用的试剂和操作 |
A | NaCl固体(Na2CO3)固体 | 加入足量盐酸,搅拌至充分反应,蒸发结晶 |
B | KCl固体(KClO3)固体 | 加入少量的MnO2,加热 |
C | CO2(CO) | 通入足量氧气,点燃 |
D | NaNO3溶液(NaOH溶液) | 加入适量CuSO4溶液,过滤 |
A.A B.B C.C D.D
K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下。下列说法不正确的是
温度 | 20 | 30 | 50 | 60 | 80 | |
溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |
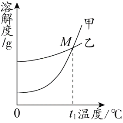
A.碳酸钾溶液中的溶剂是水
B.甲是硝酸钾的溶解度曲线
C.t1℃时,两种物质的溶解度相等
D.t1℃应在50℃~60℃之间
下表是硝酸钾和氯化铵在不同温度时的溶解度。分析表中数据,回答问题。
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 |
氯化铵 | 29.4 | 37.2 | 45.8 | 55.2 |
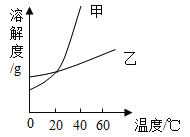
(1)上图中,甲可表示___(填化学式)的溶解度曲线。
(2)40℃时,两种物质的饱和溶液中,溶质质量分数较小的是__(填化学式)。
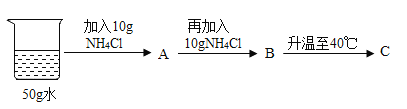
(3)20℃时,按下图所示操作,B中溶液的溶质与溶剂质量比为_____(填最简整数比);C中的溶液是__(填“饱和”或“不饱和”)溶液。
(4)60℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到60℃,剩余溶液的质量:硝酸钾溶液__(填“>”“<”或“=”)氯化铵溶液。
(5)室温下,将盛有硝酸钾的饱和溶液的试管放入盛有水的烧杯中,再向烧杯内的水中加入一定量的硝酸铵并搅拌,试管内可以观察到的现象是____。


 点燃酒精灯 B.
点燃酒精灯 B.  稀释浓硫酸
稀释浓硫酸 测溶液的pH D.
测溶液的pH D. 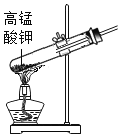 制取氧气
制取氧气