题目内容
下列实验中利用提供的方案能达到目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去CaO中混有的CaCO3 | 先加足量水,然后过滤 |
| B | 除去CO2中少量HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| C | 鉴别棉线和羊毛线 | 点燃,闻产生的气味,观察生成的灰烬 |
| D | 鉴别稀盐酸和氯化钠溶液 | 滴加酚酞溶液,观察溶液颜色变化 |
C
试题分析:A、除去CaO中混有的CaCO3,先加足量水,然后过滤,不行,因为CaO会与水反应生成氢氧化钙,改变了物质的成分,应采取高温煅烧的方法,错误,B、除去CO2中少量HCl气体,先通过NaOH溶液,再通过浓硫酸,不行,因为二氧化碳也会与NaOH溶液反应,错误,C、鉴别棉线和羊毛线,点燃,有烧纸气味的是棉线,有烧焦羽毛气味的是羊毛线,正确,D、鉴别稀盐酸和氯化钠溶液,一个呈酸性,一个呈中性,都不能使无色酚酞变红,所以滴加酚酞溶液,观察溶液颜色变化不能鉴别稀盐酸和氯化钠溶液,错误,故选C

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
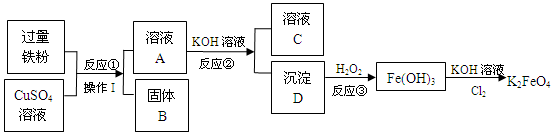
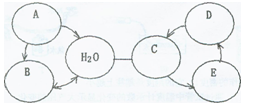
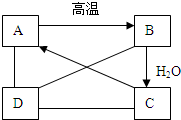

 ②2NaHCO3 Na2CO3+H2O+CO2↑
②2NaHCO3 Na2CO3+H2O+CO2↑