题目内容
合成氨工业生产中所用催化剂的主要成分是FeO和Fe2O3,且FeO与Fe2O3的质量比为9:20时,其催化活性最大.以Fe2O3为原料制备该催化剂时,可加入适量木炭粉,发生如下反应:2Fe2O3+C 4FeO+CO2↑.试计算应向160gFe2O3粉末中加入木炭粉的质量.
4FeO+CO2↑.试计算应向160gFe2O3粉末中加入木炭粉的质量.
解:设需加入木炭粉的质量是x 参加反应的Fe2O3的质量为y,生成FeO的质量为z
2Fe2O3 +C 4FeO十CO2↑
4FeO十CO2↑
320 12 288
y x z
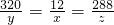
y=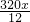 z=
z=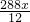
剩余Fe2O3的质量为:160g-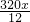 =
=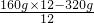
根据题意得: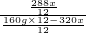 =
=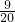
解得:x=6g
答:需加入木炭粉6g.
分析:分析题意可知当催化剂中FeO与Fe2O3的质量之比为9:20时,其催化活性最高,所以可根据反应结束后生成的FeO的质量和剩余Fe2O3的质量之比为9:20建立等式.
所以解题思路就是设出木炭的质量,根据化学方程式求出生成的FeO的质量和剩余的Fe2O3质量即可解答.
点评:解答本题的难点在于确定480gFe2O3粉末应转化为FeO的质量,因此可通过化学方程式首先确定反应中两物质的质量关系,然后再利用最佳质量比解决需要生成FeO的质量.
2Fe2O3 +C
 4FeO十CO2↑
4FeO十CO2↑320 12 288
y x z
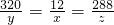
y=
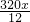 z=
z=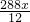
剩余Fe2O3的质量为:160g-
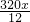 =
=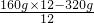
根据题意得:
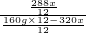 =
=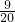
解得:x=6g
答:需加入木炭粉6g.
分析:分析题意可知当催化剂中FeO与Fe2O3的质量之比为9:20时,其催化活性最高,所以可根据反应结束后生成的FeO的质量和剩余Fe2O3的质量之比为9:20建立等式.
所以解题思路就是设出木炭的质量,根据化学方程式求出生成的FeO的质量和剩余的Fe2O3质量即可解答.
点评:解答本题的难点在于确定480gFe2O3粉末应转化为FeO的质量,因此可通过化学方程式首先确定反应中两物质的质量关系,然后再利用最佳质量比解决需要生成FeO的质量.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
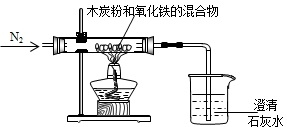
某化学活动兴趣小组的同学利用如图进行木炭还原CuO的探究实验.已知:C+2CuO
2Cu+CO2↑ C+CuO
Cu+CO↑
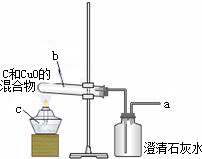
(1)该装置中试管口略向下倾斜的原因是: ;实验结束时,应 (填“先”或“后”)拔掉试管上的橡皮塞,原因是: .
(2)有同学认为该装置a处可能有CO冒出,他的理由是 .
由此,请你提出对上述C和CuO反应的装置的改进建议(只要求写两点) ; .
(3)他们通过查阅资料后,得知氧化亚铜(Cu20)为红色固体.
①请从元素守恒和元素质量分数两个方面说明生成的红色固体中可能存在氧化亚铜的原因: 、 .
②又知:Cu20能和常见的酸(HNO3除外)反应生成Cu2+和Cu、H2O;Cu不能与常见的酸(HNO3除外)反应.请你设计一个简便的实验方案,证明红色固体中含有Cu2O.
(4)已知2Fe203+3C
4Fe十3CO2↑,
如果C的量少一些,还会发生如下反应:2Fe203+C
4FeO十CO2↑
①当碳与氧化铁的质量比为 时,氧化铁会被还原成氧化亚铁;
②合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe203.
当催化剂中FeO与Fe203的质量之比为9:20时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为多少?(保留2位小数)
③以Fe203为原料制备上述催化剂,为制得这种活性最高的催化剂100g,应取Fe203粉末的质量多少克?
| ||
| ||

(1)该装置中试管口略向下倾斜的原因是:
(2)有同学认为该装置a处可能有CO冒出,他的理由是
由此,请你提出对上述C和CuO反应的装置的改进建议(只要求写两点)
(3)他们通过查阅资料后,得知氧化亚铜(Cu20)为红色固体.
①请从元素守恒和元素质量分数两个方面说明生成的红色固体中可能存在氧化亚铜的原因:
②又知:Cu20能和常见的酸(HNO3除外)反应生成Cu2+和Cu、H2O;Cu不能与常见的酸(HNO3除外)反应.请你设计一个简便的实验方案,证明红色固体中含有Cu2O.
| 实验步骤 | |
| 实验现象与结论 | |
| 化学反应方程式 |
| ||
如果C的量少一些,还会发生如下反应:2Fe203+C
| ||
①当碳与氧化铁的质量比为
②合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe203.
当催化剂中FeO与Fe203的质量之比为9:20时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为多少?(保留2位小数)
③以Fe203为原料制备上述催化剂,为制得这种活性最高的催化剂100g,应取Fe203粉末的质量多少克?
合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3.若某FeO、Fe2O3混合物中铁、氧的物质的量之比为4:5,则此混合物中Fe2O3的质量分数为( )
| A、33% | B、53% | C、67% | D、72% |