题目内容
【题目】下列有关实验,符合质量守恒定律的是( )
A.常温下,2L水与2L酒精混合后体积等于4L
B.在点燃条件下,4g红磷和5g氧气充分反应,生成9g五氧化二磷
C.在点燃条件下,2g氢气和32g氧气充分反应,生成34g水
D.在点燃条件下,32g硫和32g氧气充分反应,生成64g二氧化硫
【答案】D
【解析】
A、常温下,2L水与2L酒精混合后体积小于4L,且该过程是物理变化;故A错误;
B、P和O2点燃生成P2O5的反应化学方程式是:在4P+5O2![]() 2P2O5中,由方程式可知,P、O2、P2O5的质量比为124:160:284=31:40:71,生成9g的五氧化二磷,需要磷和氧气的质量分别为3.9g、5.1g,故错误;
2P2O5中,由方程式可知,P、O2、P2O5的质量比为124:160:284=31:40:71,生成9g的五氧化二磷,需要磷和氧气的质量分别为3.9g、5.1g,故错误;
C、氢气在氧气中燃烧的化学方程式为
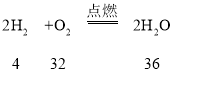
参加反应的氢气、氧气与生成的水的质量比为4:32:36,则2g氢气能与16g氧气完全反应生成18g水,反应后氧气有剩余,故错误;
D、反应中硫、氧气、二氧化硫质量比为32:32:64=1:1:2,32g硫和32g氧气恰好完全反应生成64g二氧化硫,故正确。
故选:D。

 高中必刷题系列答案
高中必刷题系列答案【题目】碱石灰是实验室常用的干燥剂。实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物,极易吸收空气中的水蒸汽和CO2。
(提出问题)实验室中久置的碱石灰样品的成分是什么?
(查阅资料)CaCl2溶液呈中性。
(进行猜想)久置碱石灰样品中可能含有CaO、NaOH、Ca(OH)2、Na2CO3、CaCO3中的两种或两种以上成分。样品中可能含有Ca(OH)2、Na2CO3的原因是(请用化学方程式表示)_____、_____。
(实验过程)某实验小组对久置碱石灰的成分进行实验,以下是实验报告的一部分,请你用所学知识分析并填空。
操作 | 现象 | 结论 | |
(1)取一定量碱石灰样品于小烧杯,加入足量水,搅拌 | 形成悬浊液 | ||
(2)将(1)所得混合物过滤,在滤渣中加入稀盐酸 | 有气泡产生 | ①滤渣中一定含有_____ | |
将所得溶液分为三等份 | (3)第一份滤液中通入足量的CO2. | 无明显现象 | ②滤液中一定不含_____、_____ ③滤液中一定含_____ |
(4)第二份滤液中滴入足量澄清石灰水 | 有沉淀产生 | ||
(5)第三份滤液中滴入过量的CaCl2溶液,静置后,在上层清液中滴加酚酞试液. | 产生白色沉淀,酚酞试液不变色 | ||
(实验结论)根据上述实验分析得出结论:该碱石灰样品的组成为_____(填化学式).