��Ŀ����
����Ŀ��������̽���������غ㶨�ɡ��Ľ�ѧƬ�Σ��������̽������д�ո�
��������⡿��ѧ��Ӧǰ������ʵ������ܺ��Ƿ���ȣ�
����������衿����1������ȣ� ����2����ȡ�
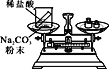
��ʵ��̽�����ס�������ͬѧ��������ƽ�ֱ������Ӧǰ�����ʵ�������
�� �� | �� �� | |
ʵ�鷽������Ӧ���ԣ� |
|
|
ʵ�� ���� | �����ݲ����� ��ƽָ������ƫת | ���������к�ɫ���������� ��Һ��ɫ�����ı䣬 ��ƽָ��û��ƫת |
���� | ����1��ȷ ��Ӧ�Ļ�ѧ����ʽ���� | ����2��ȷ ��Ӧ�Ļ�ѧ����ʽ���� |
д������ʵ���еĻ�ѧ����ʽ����________________________________________��
��___________________________________________________��
����˼���ۡ��������ֲ�����ȷ��ͨ�����ۣ�ͬѧ�Ƿ��ּ��������������������ָ������ƫת���õ���ʾ����̽����ѧ��Ӧǰ������ʵ������ܺ��Ƿ����ʱ�������������ɻ�μӵķ�Ӧһ��Ҫ��_______________�н��С�
���Ż�װ�á�ͬѧ�ǶԼ��������еķ�Ӧװ�ý������������ָĽ�������Ϊ���װ����______������ţ�����������װ�õIJ���֮���ֱ��ǣ�________��________��
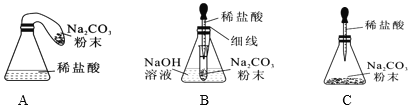
���ó����ۡ�ͬѧ�����øĽ�������װ�ý����ٴ�̽�������ó��������ȷ����һ���������֣���Ӧ��ϵ�����ĺ�δ�μӷ�Ӧ�����ʵ������ڷ�Ӧǰ�ֲ��䣬���յó����ۣ�________�ĸ����ʵ������ܺ͵��ڷ�Ӧ�����ɵĸ����ʵ������ܺ͡�
������Ӧ�á����ͣ���ѧ��Ӧǰ��ԭ�ӵ����ࡢ��Ŀ�����������䣬���������غ㡣
Ӧ�ã�ij�����������Ȼᷢ���ֽⷴӦ����������ͭ��ˮ�Ͷ�����̼�������ʣ���ù��������к��е�Ԫ����______________________������Ԫ�ط��ţ�
���𰸡� Na2CO3+2HCl=2NaCl+H2O+ CO2�� Fe + CuSO4 == FeSO4 + Cu �ܱ�������������ϵ�Ⱥ����𰸣� B Aװ���з�Ӧ�������壬�������ͣ����������³�������� Cװ���з�Ӧ�������壬ƿ����ѹ�����ܵ���ƿ�����������������Ҳ�ɣ� �μӻ�ѧ��Ӧ����μӷ�Ӧ�� C��H��O��Cu
����������ʵ��̽�����ٷ�Ӧ�Ļ�ѧ����ʽΪ��Na2CO3+2HCl=2NaCl+H2O+ CO2������Ӧ�ڵĻ�ѧ����ʽΪ��Fe + CuSO4 == FeSO4 + Cu ����˼���ۡ���̽����ѧ��Ӧǰ������ʵ������ܺ��Ƿ����ʱ�������������ɻ�μӵķ�Ӧһ��Ҫ���ܱ������н��С����Ż�װ�á����װ����B��Aװ���з�Ӧ�������壬�������ͣ����������³�������� ��Cװ���з�Ӧ�������壬ƿ����ѹ�����ܵ���ƿ����������ó����ۡ��μӻ�ѧ��Ӧ�ĸ����ʵ������ܺ͵��ڷ�Ӧ�����ɵĸ����ʵ������ܺ͡�������Ӧ�á���ѧ��Ӧǰ�����Ԫ�ص�����䡣

 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�����Ŀ���������и������ʵķ�������ȷ����
ѡ�� | ��������� | ����ķ��� |
A | ��ˮ�Ϳ�Ȫˮ | �۲��Ƿ���� |
B | ������̼��һ����̼ | ��ȼ���۲��Ƿ���ȼ�� |
C | ˮ����������Һ | �Ӷ������̣��۲��Ƿ������� |
D | ���ɱ� | ���£�20�棩���ã���һ��ʱ��۲��Ƿ���Һ����� |
A. A B. B C. C D. D