题目内容
 探究碳酸氢钠的热稳定性
探究碳酸氢钠的热稳定性
【查阅资料】碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质.
【进行实验】为验证碳酸氢钠受热时会分解,兴趣小组的同学取一定
质量的碳酸氢钠放在铜片上加热,如右图所示.
(1)加热一段时间后,观察到烧杯内壁有______.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式:______.
(3)兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3.
①他们猜想的依据是______.
②设计实验,检验反应后的固体产物是Na2CO3而不是NaOH,并填入下表
| 实 验 操 作 | 预期实验现象 | 结 论 |
| ______ | ______ | 固体产物是Na2CO3,而不是NaOH. |
解:(1)碳酸氢钠受热能生成水,故烧杯内壁有水珠出现;
(2)碳酸氢钠受热能分解生成二氧化碳,能与氢氧化钙反应生成碳酸钙沉淀和水,方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(3)①根据质量守恒定律,化学反应前后元素的种类不变,所以本题答案为:根据质量守恒定律,反应前后元素的种类不变;
②要检验碳酸钠的存在,且不是氢氧化钠存在,可采用让碳酸根转化为沉淀,并采用酚酞试液检验溶液是否是反应后呈碱性的方法排除氢氧化钠的存在(答案只要合理即可)
故答案为:(1)水珠;
(2)Ca(OH)2+CO2=CaCO3↓+H2O;
(3)①根据质量守恒定律,反应前后元素的种类不变;
②
分析:根据质量守恒定律,化学反应前后元素的种类不变,可以根据碳酸氢钠所含有的元素种类猜测生成物质的化学式,根据生成的物质的特点回答实验中出现的实验现象,二氧化碳与氢氧化钙反应生成碳酸钙和水,碳酸盐能与酸反应生成二氧化碳,要检验碳酸钠,可以使用加酸化气的方法.
点评:本题主要考查物质的酸碱性和化学方程式的书写等方面的知识,本题要求学生在熟练掌握化学基本知识的基础上,提高学生结合课本知识分析问题解决问题的能力,是一道不错的综合题.
(2)碳酸氢钠受热能分解生成二氧化碳,能与氢氧化钙反应生成碳酸钙沉淀和水,方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(3)①根据质量守恒定律,化学反应前后元素的种类不变,所以本题答案为:根据质量守恒定律,反应前后元素的种类不变;
②要检验碳酸钠的存在,且不是氢氧化钠存在,可采用让碳酸根转化为沉淀,并采用酚酞试液检验溶液是否是反应后呈碱性的方法排除氢氧化钠的存在(答案只要合理即可)
故答案为:(1)水珠;
(2)Ca(OH)2+CO2=CaCO3↓+H2O;
(3)①根据质量守恒定律,反应前后元素的种类不变;
②
| 实 验 操 作 | 预期实验现象 | 结 论 |
| 取样,滴加过量的CaCl2溶液,充分反应后过滤,在滤液中滴加酚酞 | 产生白色沉淀,滤液不变红 | 固体产物是Na2CO3,而不是NaOH. |
分析:根据质量守恒定律,化学反应前后元素的种类不变,可以根据碳酸氢钠所含有的元素种类猜测生成物质的化学式,根据生成的物质的特点回答实验中出现的实验现象,二氧化碳与氢氧化钙反应生成碳酸钙和水,碳酸盐能与酸反应生成二氧化碳,要检验碳酸钠,可以使用加酸化气的方法.
点评:本题主要考查物质的酸碱性和化学方程式的书写等方面的知识,本题要求学生在熟练掌握化学基本知识的基础上,提高学生结合课本知识分析问题解决问题的能力,是一道不错的综合题.

练习册系列答案
相关题目
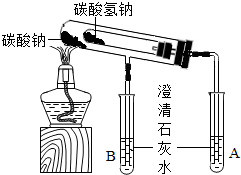
 17、17、研究性学习小组对碳酸钠和碳酸氢钠的性质进行探究,请你参与实验.
17、17、研究性学习小组对碳酸钠和碳酸氢钠的性质进行探究,请你参与实验.
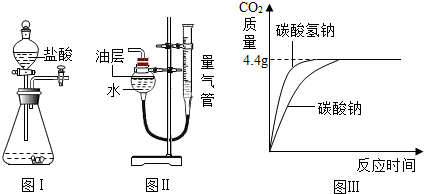
 (2012?河西区二模)校兴趣小组对碳酸钠和碳酸氢钠的性质进行进研究,请你参与并完成相关问题.
(2012?河西区二模)校兴趣小组对碳酸钠和碳酸氢钠的性质进行进研究,请你参与并完成相关问题.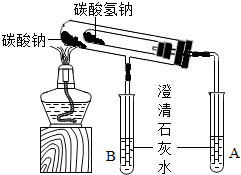 校兴趣小组对碳酸钠和碳酸氢钠的性质进一步研究,请你参与并完成相关问题.
校兴趣小组对碳酸钠和碳酸氢钠的性质进一步研究,请你参与并完成相关问题.
