题目内容
【题目】实验室有一包含杂质的碳酸氢钠样品50g(杂质不含钠元素,受热不变化),其中钠元素的质量分数为23%,180℃时,将样品加热一段时间后称得固体质量为43.8g,则分解的碳酸氢钠占原碳酸氢钠的质量分数为(已知![]() )
)
A.60%B.47.3%C.40%D.33.6%
【答案】C
【解析】
原混合物中钠元素的质量:50g×23%=11.5g。
通过钠元素的质量可以计算出原碳酸氢钠的质量为:11.5g÷![]() =42g。
=42g。
加热一段时间后固体质量为43.8g,则减少的质量为:50g-43.8g=6.2g。
减少的6.2g是生成的水和二氧化碳的质量。
社分解碳酸氢钠的质量为x,则根据差量法有:

解得x=16.8g
分解的碳酸氢钠占原碳酸氢钠的质量分数为:![]() 。
。
故选C。

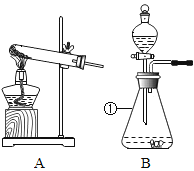
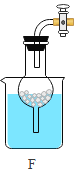
【题目】有如下图所示的两个实验:
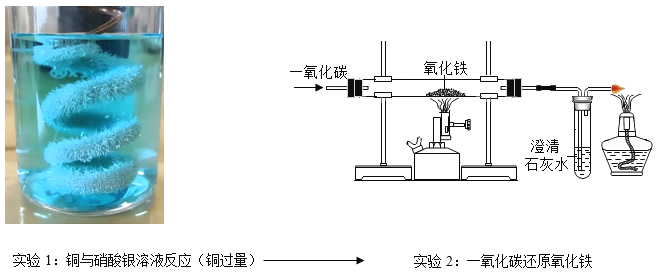
(1)在实验 2 中,加热硬质玻璃管时,管中发生反应的化学方程式为_____。
某同学取一些实验 1 反应后的溶液和一些实验 2 反应后硬质玻璃管中的固体,将它们一同倒入容器M 中,发现有明显变化现象产生,且最终还有固体存在。他对 M 中反应后的物质成分进行如下探究。
(查阅资料)Fe2O3 + 6HCl = 2FeCl3 + 3H2O(FeCl3 溶液呈黄色);Fe2O3 与 Cu(NO3)2 不反应。
(实验分析)M 中一定发生了的反应的化学方程式是_____。
(提出猜想)反应后,M 中剩余的固体是什么?
猜想Ⅰ:Cu 和 Fe 猜想Ⅱ:Cu 和 Fe2O3 猜想Ⅲ:______。
(进行实验)进行如下实验,请完成填空。
实验步骤 | 实验现象 | 实验结论 |
一、把 M 中反应后的混合物过滤, 得到固体和溶液,将固体烘干, 用磁铁吸引固体。 | ______ | 固体中不含铁。 |
二、再取少量步骤一的固体,加 入过量的稀盐酸。 | 固体减少,溶液变成黄色 | 固体中一定含有_____。 |
(问题探讨)
(2)从 M 中滤出的固体不含单质铁的原因是_________。
(3)如果要进一步确定容器 M 滤出的溶液中是否含有硝酸铜,可用 __________(填试剂名称) 进行检验,通过 __________的现象来进行判断。