题目内容
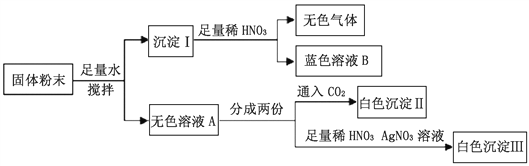
【题目】一包固体粉末可能含有Mg(NO3)2、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,某同学设计了如下实验方案,下列判断正确的是
A. 沉淀Ⅰ是氢氧化铜沉淀
B. 无色溶液A中一定有NaOH
C. 原固体粉末肯定有NaCl
D. 原固体粉末一定有CaCO3、NaOH、Mg(NO3)2、CuCl2和Ca(NO3)2
【答案】B
【解析】根据“一包固体粉末可能含有Mg(NO3)2、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种”,结合图框,则推测铜离子在溶液中显蓝色,NaOH和CuCl2会生成氢氧化铜沉淀,而氢氧化铜沉淀与稀硝酸反应生成硝酸铜溶液;CaCO3和硝酸反应会生成气体,则蓝色溶液B中有硝酸铜、硝酸钙、硝酸钠、稀硝酸,而原固体粉末一定有CaCO3、NaOH、CuCl2和Ca(NO3)2,无法确定是否含有NaCl;Mg(NO3)2。
A.由分析可知,沉淀Ⅰ中有氢氧化铜沉淀和CaCO3沉淀,故错误;
B. 无色溶液A中一定有NaOH,正确;
C. 原固体粉末是否有NaCl,无法确定,故错误;
D. 原固体粉末一定有CaCO3、NaOH、CuCl2和Ca(NO3)2,故D错误。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目