题目内容
【题目】运用广泛的金属材料是钢铁,如图是冶炼生铁相关流程。请认真读图回答问题:
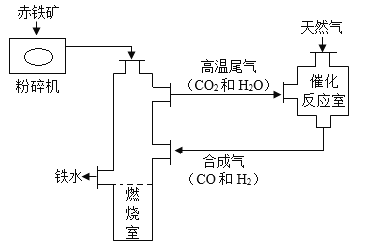
(1)高炉冶炼生铁的原料有铁矿石、焦炭和_____。 冶炼时将原料粉碎后再使用的原因是_____。
(2)焦炭在冶炼中的作用为①提供高温,②_____。赤铁矿(主要成分Fe2O3)炼铁的反应原理是_____。
(3)炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是_____。
(4)钢铁的锈蚀造成极大的损失和浪费。但如果将“铁生锈”原理应用得当,同样可以造福人类,请举例_____(写一条)。
【答案】石灰石 增大反应物接触面积,充分反应 产生还原剂CO ![]() +4 食品保鲜剂(合理即可)
+4 食品保鲜剂(合理即可)
【解析】
(1)高炉冶炼生铁的原料有铁矿石、焦炭和石灰石;冶炼时将原料粉碎后再使用是为了增大反应物接触面积,充分反应;
(2)焦炭燃烧放出热量;在高温的条件下,焦炭与二氧化碳反应生成具有还原性的一氧化碳气体;在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳;化学方程式为: ![]() ;
;
(3)钙元素显+2价,氧元素显﹣2价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+x+(﹣2)×3=0,则x=+4价;
(4)铁会与氧气、水反应而生锈,所以如果将“铁生锈”原理应用得当,同样可以造福人类,如:食品的保鲜剂、制成暖宝等。

 华东师大版一课一练系列答案
华东师大版一课一练系列答案【题目】为了解某NaCl、Na2CO3固体混合物中Na2CO3与盐酸的反应情况,张南同学取16g该混合物放入烧杯中,分五次加入稀盐酸(每次加入稀盐酸的质量为25g),待反应完全后,得到下表中相关数据,请分析表格中数据,回答下列问题。
加入稀盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
烧杯及反应后混合物的总质量/g | 122.2 | 146.1 | 170.0 | 193.9 | 218.9 |
(1)写出发生反应的化学方程式___;
(2)列出求解该混合物中碳酸钠质量(x )的比例式___;
(3)前三次加酸后参加反应碳酸钠质量占原混合物中碳酸钠质量的百分比为___;
(4)当加入稀盐酸至固体混合物恰好完全反应时,若向所得不饱和溶液中加入59.4g蒸馏水,最终所得溶液中溶质的质量分数是___;
(5)若用36.5%的浓盐酸配制上述所需要的盐酸,则需要加水的质量为___。