题目内容
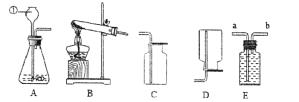
【题目】为了测定某品牌纯碱样品中碳酸钠的质量分数(假设该样品中只含有氯化钠一种杂质),兴趣小组进行了如下图所示的是实验,请你分析并计算:
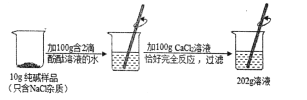
(1)恰好完成反应时可观察到的现象;
(2)样品中碳酸钠的质量分数.
【答案】(1)溶液由红色变成无色;(2)84.8%
【解析】 Na2CO3 + CaCl2 == CaCO3↓+ 2NaCl(1)恰好反应时,溶液呈中性,酚酞遇碱性溶液变红,遇酸性或中性溶液不变色,故恰好反应时的现象是溶液由红色变成无色。(2)根据质量守恒定律,反应过滤后减少的质量是生成碳酸钙的质量:10g+100g+100g-202g=8g,设样品中碳酸钠的质量为x。
Na2CO3 + CaCl2 == CaCO3↓+ 2NaCl
106 100
x 8g
![]() =
=![]() ,解得x=84.8%
,解得x=84.8%

 阅读快车系列答案
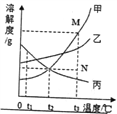
阅读快车系列答案【题目】下图是用氯化钠溶液和氯化钾溶液制取氯酸钾的工艺流程,请根据题意回答下列问题。
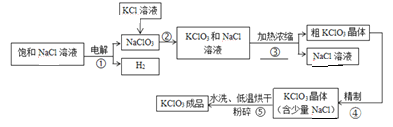
【资料】氯酸钾和氯化钠部分温度下的溶解度如下:
10℃ | 20℃ | 30℃ | 40℃ | |
氯酸钾 | 5.0g | 7.4g | 10.0g | 14.0g |
氯化钠 | 35.8g | 36.0g | 36.3g | 36.6g |
(1)请写出步骤②的化学方程式_________,该反应的基本反应类型是_________________。
(2)步骤③的操作分别是_________、过滤(填操作名称)。
(3)步骤⑤中是采用20℃以下的水进行洗涤,目的是①除去少量氯化钠②_____________。
(4)步骤⑤采用低温烘干,为什么不采用高温烘干___________________________(用化学方程式表示)。
【题目】学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200 g,平均分成4份进行实验,结果如下:
实验 | 一 | 二 | 三 | 四 |
加入样品的质量/g | 5 | 10 | 15 | 20 |
生成的CO2质量/g | 1.76 | 3.52 | 4.4 | m |
(1)上表中m的数值是 ;
(2)反应中矿石有剩余是第 次实验;
(3)这种石灰石矿中碳酸钙的质量分数是 ;
(4)稀盐酸中溶质的质量分数是 .