题目内容
小明在探究稀盐酸与氢氧化钠溶液能否发生中和反应时,先向氢氧化钠溶液中滴入两滴 ,原因是 .然后逐滴滴加稀盐酸至溶液刚好由 色变为 色,证明两种溶液恰好反应,溶液中溶质是 (化学式).
考点:中和反应及其应用
专题:常见的酸 酸的通性
分析:根据碱能使酚酞试液变红,酸不能使酚酞试液变色,氯化钠属于中性物质,不能使酚酞试液变红.
解答:解:由于碱能使酚酞试液变红,所以氢氧化钠溶液中滴入无色酚酞试液变为红色;由于氢氧化钠属于碱pH>7,然后逐滴滴加稀盐酸至溶液刚好由由红色变为无色,氢氧化钠与盐酸恰好反应生成氯化钠,溶液显中性.
答案:无色酚酞试液;碱能使酚酞试液变红; 红;无;NaCl
答案:无色酚酞试液;碱能使酚酞试液变红; 红;无;NaCl
点评:解答本题关键是要知道酸和中性溶液都不能使酚酞试液变色,碱能使酚酞试液变红.

练习册系列答案
相关题目
下列物质的组成中不含有原子团的是( )
| A、Na2SO4 |
| B、Mg(OH)2 |
| C、NaCl |
| D、CaCO3 |
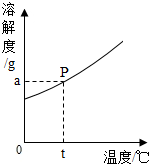 实验室配制氯化铵(NH4Cl)溶液不能使用硬水,因硬水中含有较多的
实验室配制氯化铵(NH4Cl)溶液不能使用硬水,因硬水中含有较多的