题目内容
【题目】化学方程式符合题意且书写正确的是
A. 用止酸剂Al(OH)3治疗胃酸过多:Al(OH)3+HCl→AlCl+3H2O
B. 除去CO中混有的CO2,通过灼热CuO:CO+CuO![]() Cu+CO2
Cu+CO2
C. 用氢氧化钠溶液吸收尾气中二氧化硫:2NaOH+SO2→Na2SO4+H2O
D. 用稀硫酸除铁锈:Fe2O3+3H2SO4→Fe2(SO4)3+3H2O
【答案】D
【解析】A、书写化学方程式的依据是质量守恒定律,书写步骤是:一写二配三标四查。A、氯化铝的化学式书写错误;B、除去CO中混有的CO2,不能通过灼热CuO,否则会把一氧化碳除去,可将混合气体通过氢氧化钠溶液,错误;C、二氧化硫与氢氧化钠反应生成的是氩硫酸钠,错误;D、稀硫酸除铁锈是的是硫酸铁和水,正确。故选D。

 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案【题目】镍粉常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
I、【镍粉制备】:
工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体xNiCO3·yNi(OH)2·zH2O,并利用其制备镍粉的流程如下:
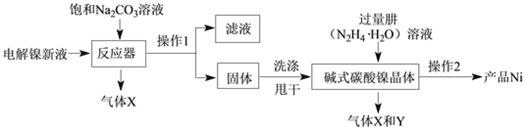
(1)反应器中的一个重要反应为3NiSO4 + 3Na2CO3 + 2H2O = NiCO3·2Ni(OH)2 +3Na2SO4 + 2X,X的化学式为______。
(2)物料在反应器中反应时需要控制反应条件。
分析下图,反应器中最适合的温度及pH分别为______℃、______。
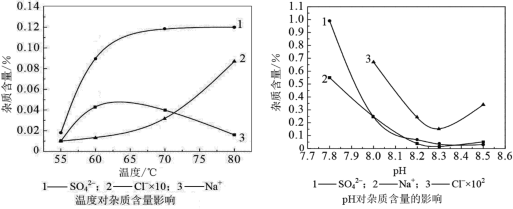
(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将______(填“升高”、“降低”或“不变”)。
(4)操作1的名称是_______________,实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒及_________,其中玻璃棒的作用是_____。
(5)固体洗涤时,需用纯水洗涤,检验其洗涤干净的试剂是______。
(6)气体Y是空气中含量最多的气体,其是______(填名称)。
(7)操作2含过滤、水洗、95%酒精浸泡、晾干等操作,其中用95%酒精浸泡的目的是______。
II、【测定碱式碳酸镍晶体的组成】:为测定碱式碳酸镍晶体(xNiCO3·yNi(OH)2·zH2O)组成,某小组设计了如下实验方案及装置:
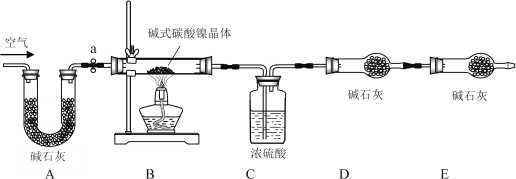
【资料卡片】:
①碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O。
②400℃左右,NiO会氧化生成Ni2O3。
③碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O。
【实验步骤】:
①______;②准确称取3.77g xNiCO3·yNi(OH)2·zH2O放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,称量装置C、D的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,______;⑥准确称量装置C、D的质量;⑦根据数据进行计算(相关数据如表)。
装置C / g | 装置D / g | 装置E / g | |
加热前 | 200.00 | 180.00 | 180.00 |
加热后 | 201.08 | 180.44 | 180.00 |
【实验分析及数据处理】:
(8)完善实验步骤中的填空:①______;⑤______。
(9)计算xNiCO3·yNi(OH)2·zH2O中x:y:z的值______。
(10)左侧通空气的目的是______、______。
【实验反思】:
(11)实验结束后,称得装置B中残留固体质量为2.33g。请通过计算确定残留固体的组成及各成分的质量(写出计算过程,精确到小数点后两位)_____。




