题目内容
【题目】为探究分子的运动及影响分子运动速率的因素,某同学设计了以下三种实验方案,请回答有关问题。
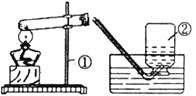
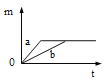
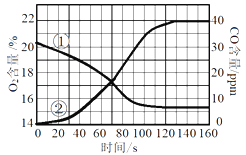
(实验方案一)如图1。
(1)观察到的实验现象是__________;
(2)该方案的不足之处是__________。(说出一点即可)
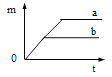
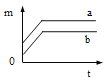
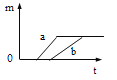
(实验方案二)如图2、图3。
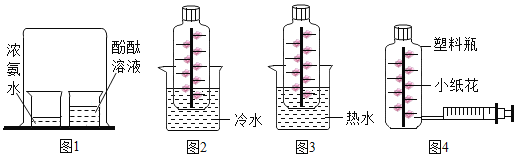
图中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图4的操作方式分别用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。观察到的现象是____________;
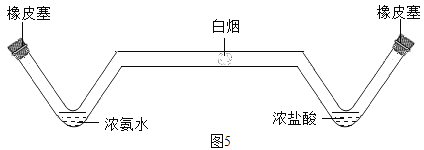
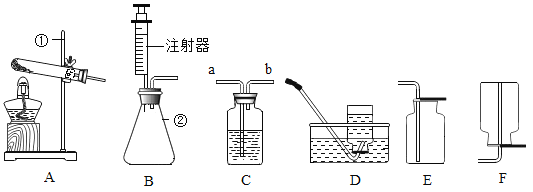
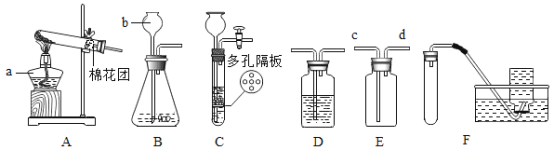
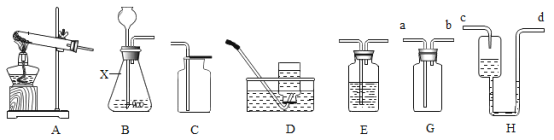
(实验方案三)如图5(盐酸是HCl气体的水溶液)
用长柄V形玻璃管进行实验,向左、右两端的V形玻璃管口分别同时滴入等量的浓氨水和浓盐酸,塞紧橡皮塞。过一会儿后,从图5中观察到有白烟产生且位置偏右,说明_________。
若用“![]() ”表示氢原子,用“
”表示氢原子,用“![]() ”表示氮原子,用“
”表示氮原子,用“![]() ”表示氯原子,上述反应过程可表示为(图2所示):
”表示氯原子,上述反应过程可表示为(图2所示):
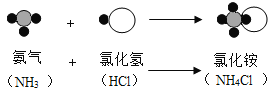
氨气的化学式为NH3,你能从中了解到哪些信息_______(任写一条)。则该反应的符号表达式为:_________,
分析以上微观模拟图,你能得出的结论有(任写一条)__________。
(实验结论)上述实验证明:分子是不断运动的,且分子的运动速率与_______有关。(说出一点即可)
【答案】B烧杯中液体由无色变为红色 没有设计对比实验 两个塑料瓶中纸花由下而上依次变红,且热水中的纸花先变红 分子在运动,且氨分子运动速率比氯化氢分子运动速率快 氨气是由氮元素和氢元素组成(其他答案合理亦可) NH3+HCl=NH4Cl 原子是化学变化中的最小粒子(其他答案合理亦可) 温度(或分子的质量)
【解析】
[实验方案一]
①观察到的实验现象是酚酞试液变红色。
故填:B烧杯中酚酞试液由无色变为红色。
②该方案的不足之处是没有设计对比实验,不能排除空气中的物质使酚酞溶液变色。
故填:没有设计对比实验。
[实验方案二]
①观察到的现象是两个塑料瓶中纸花由下而上依次变红,且热水中的纸花先变红。
故填:两个塑料瓶中纸花由下而上依次变红,且热水中的纸花先变红。
[实验方案三]
①过一会儿后,从图5中观察到有白烟产生且位置偏右,说明氯化氢和氨气发生了化学反应,氨分子运动的比氯化氢分子运动的快。
故填:氯化氢和氨气发生了化学反应,氨分子运动的比氯化氢分子运动的快。
氨气的化学式为NH3,能从中了解到的信息是一个氨气分子由一氮原子和三个氢原子构成;
由微观模拟图2可知,该反应是氨气与氯化氢气体反应生成了氯化铵,符号表达式为:NH3+HCl=NH4Cl;由微粒的变化可知,原子的种类及数目在化学变化中不会改变;
故填:一个氨气分子由一氮原子和三个氢原子构成;NH3+HCl=NH4Cl;原子的种类及数目在化学变化中不会改变。
[实验结论]
上述实验证明:分子是不断运动的,且分子的运动速率与温度(或分子的质量)。
故填:温度(或分子的质量)。

【题目】小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加.
[知识回放]
金属活动性顺序:K Ca Na Mg Al Zn Sn Pb(H) Hg Ag Pt Au,请你在横线上填写对应金属的元素符号.
[作出猜想]
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是 .
[查阅资料]
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
[设计实验]
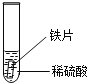
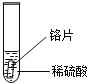
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
实验 | 试管1 | 试管2 | 试管3 |
实验 操作 |
|
|
|
实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 |
|
[结论与解释]
(1)小聪得到的结论是猜想 正确.
(2)实验前用砂纸打磨金属片的目的是 .
[知识运用]
将铬片投入FeSO4溶液中,反应 (填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式 .