题目内容
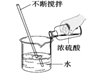
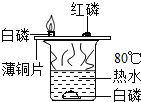
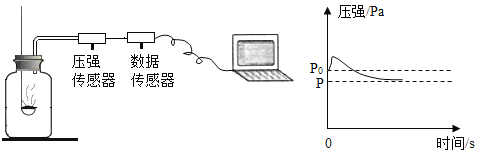
【题目】(1)为测定空气中氧气的含量,左下图所示实验装置气密性良好,与集气瓶相连的压强传感器等电子设备可将集气瓶内气体压强精确地记录并保存下来;右下图是实验过程中集气瓶内的压强变化曲线。
①写出红磷燃烧的化学方程式_______________。
②根据上图请描述红磷燃烧开始后,集气瓶内压强随时间变化的情况是______,原因是_________。
③若燃烧匙内所装红磷的量偏少,则测出的氧气的含量偏______(填“低”或“高”)。
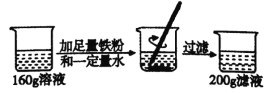
(2)小明用容积为125 mL的集气瓶通过向上排空气法收集二氧化碳气体。验满后小明认为这瓶气体不是纯净的,为测定这瓶气体中二氧化碳的体积分数,设计如图装置进行实验(装置气密性良好)。
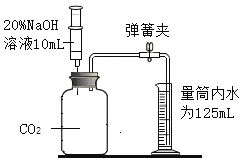
(查阅资料)氢氧化钠(NaOH)可以与二氧化碳反应,生成碳酸钠(Na2CO3)和水,碳酸钠易溶于水,写出反应的化学方程式_________________。
(实验操作)将注射器内的氢氧化钠溶液全部注入集气瓶中,轻轻地稍微振荡集气瓶,打开弹簧夹,量筒内的水沿导管流入集气瓶,实验结束后,经检验集气瓶内氢氧化钠有剩余,并测得集气瓶外剩余的水35 mL。
(实验结果)这瓶气体中二氧化碳的体积分数=________________。
(反思与评价)该实验还存在误差,原因可能是_______________。
【答案】4P+5O2![]() 2P2O5 压强先增大后减小 红磷燃烧放出热量,反应消耗氧气,反应后温度降低 低 CO2+2NaOH=Na2CO3+H2O 80% 塞瓶塞时部分二氧化碳逸出集气瓶
2P2O5 压强先增大后减小 红磷燃烧放出热量,反应消耗氧气,反应后温度降低 低 CO2+2NaOH=Na2CO3+H2O 80% 塞瓶塞时部分二氧化碳逸出集气瓶
【解析】
(1)
①红磷燃烧产生大量白烟,生成五氧化二磷,方程式故填4P+5O2![]() 2P2O5;
2P2O5;
②由图可知压强先增大后减小,故填压强先增大后减小;红磷燃烧放出热量使集气瓶内气体体积膨胀,所以压强先变大,反应结束后,集气瓶内氧气被消耗,温度逐渐降低,压强减小,故填红磷燃烧放出热量,反应消耗氧气,反应后温度降低;
③若红磷的量不足,不能耗尽集气瓶内氧气,使测得的结果偏低,故填低;
(2)
[查阅资料]
氢氧化钠(NaOH)与二氧化碳反应生成碳酸钠(Na2CO3)和水,碳酸钠易溶于水,反应的化学方程式故填CO2+2NaOH=Na2CO3+H2O;
[实验结果]
集气瓶容积为125mL,由题意知进入集气瓶液体体积为(125+10-35)mL=100mL,即反应掉的二氧化碳体积,所以这瓶气体中二氧化碳的体积分数=![]() ×100%=80%,故填80%;
×100%=80%,故填80%;
[反思与评价]
装置气密性良好,实验还存在误差,可能会有部分二氧化碳在塞瓶塞时逸出集气瓶,故填塞瓶塞时部分二氧化碳逸出集气瓶。

【题目】分类、类比推理都是学习化学常用的方法。
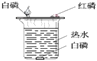
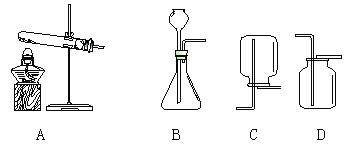
(1)在A、B、C、D实验中,某些实验设计的原理是相同的。
稀释浓硫酸 | 探究燃烧条件 | 探究中和反应 | 探究铁钉生锈 |
|
|
|
|
A | B | C | D |
其中实验B与_____(填字母)归为一类,依据是它们都采用____________的科学方法。
(2)过量的CO2能与Ca(OH)2反应如下: Ca(OH)2+2CO2==Ca(HCO3)2;

同理过量的CO2也能与NaOH反应:NaOH+CO2==NaHCO3
写出侯德榜(如图纪念邮票)制碱法的第一步反应:向氨水中通入过量的CO2反应的化学方程式为_____________________;在第二步利用减压蒸发方法获取副产品NH4Cl,在当时,它的用途是用作_________,这也是侯德榜对人类的贡献之一。