题目内容
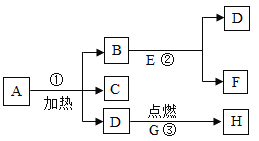
【题目】根据下列实验装置图,回答有关问题,
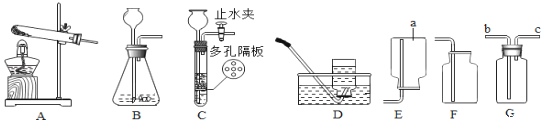
(1)装置图中仪器 a 的名称为___。
(2)若选择高锰酸钾制取并收集较纯净的O2,则应选择装置组合_____,反应的化学 方程式是:___,连接好仪器之后,首先应该进行的操作是___,该套装置有一处不足的地方,应该进行的改进是:___。
(3)小明在实验室用锌粒和稀硫酸制取并收集干燥的氢气,应可选用的装置组合是___,写出发生反应的化学方程式___。如果利用G装置收集氢气,气体应从___端通入(填“b”或“c”)。
(4) 用块状固体和液体常温下制取气体时,经常用C代替B,和B 装置相比,C装置的优点 是___;
(5) 实验室用CaC2固体和水反应制取乙炔(化学式为 C2H2),同时生成氢氧化钙。请写出实验 室制取乙炔气体的化学方程式___。
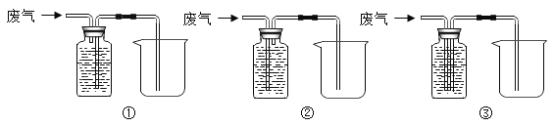
(6)某小组的同学收集到了含CO和CO2的废气,经过讨论认为废气中CO可以再利用。于是设计如下装置除去废气中的CO2,并收集一瓶CO,准备进行后续地探究。 其中最合理的装置是___(填序号)。(提示:瓶内为氢氧化钠溶液,可以除去CO2)
【答案】集气瓶 AD 2KMnO4![]() K2MnO4 +MnO2 +O2↑ 检查装置的气密性 试管口放一团棉花 BE或CE Zn +H2SO4=ZnSO4+H2↑ c 能控制反应的发生与停止 CaC2 +2H2O=Ca(OH)2+C2H2↑ ③
K2MnO4 +MnO2 +O2↑ 检查装置的气密性 试管口放一团棉花 BE或CE Zn +H2SO4=ZnSO4+H2↑ c 能控制反应的发生与停止 CaC2 +2H2O=Ca(OH)2+C2H2↑ ③
【解析】
(1)根据所学仪器的名称和用途,a的名称是集气瓶;
故填:集气瓶;
(2)用高锰酸钾制取氧气,是高锰酸钾在加热的条件下反应生成锰酸钾、二氧化锰和氧气;收集较纯净的氧气,应采用排水法收集氧气,故选择的组合是AD,反应的化学方程式是![]() ,仪器连接好之后,要检查装置的气密性,用高锰酸钾粉末制取气体,在试管口放一团棉花,防止高锰酸钾粉末进入导管,堵塞导管;
,仪器连接好之后,要检查装置的气密性,用高锰酸钾粉末制取气体,在试管口放一团棉花,防止高锰酸钾粉末进入导管,堵塞导管;
故填:AD ![]() 检查装置的气密性 在试管口放一团棉花。
检查装置的气密性 在试管口放一团棉花。
(3)实验室用锌粒和稀硫酸反应生成硫酸锌和氢气,锌粒是固体,稀硫酸是液体,应选择固体和液体反应制取气体的发生装置,收集干燥的氢气,不能用排水法收集,氢气的密度比空气的小,应采用向下排空气法收集氢气,可选择BE或CE,反应的化学方程式是![]() ,用G装置收集氢气,氢气的密度比空气的小,氢气从导管口在上的c端管口进气;
,用G装置收集氢气,氢气的密度比空气的小,氢气从导管口在上的c端管口进气;
故填: BE或CE ![]() c。
c。
(4)C装置具有的优点是可以控制反应的发生与停止;
故填:能控制反应的发生与停止。
(5)CaC2固体和水反应制取乙炔(化学式为 C2H2),同时生成氢氧化钙,反应的化学方程式是![]() ;
;
故填:![]() 。
。
(6)收集到含CO和CO2的废气,要除去CO2,可把混合气体通过氢氧化钠溶液,CO有毒,不能排放到空气中,可把混合气体通过氢氧化钠溶液吸收CO2,再利用气体产生的压强把氢氧化钠溶液排到烧杯中,故可选择③;
故填③。

【题目】铁、铝、铜是常见的三种金属。同学们发现生活中的铝制品和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理。
(提出问题)这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
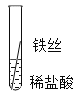
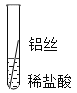
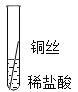
(实验探究)同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格。将粗细相同的铁丝、铝丝、铜丝分别插入稀盐酸中。
操 作 |
|
|
| 根据现象得出金属活动性顺序 |
片刻后的现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
几分钟后的现象 | 有少量气泡 | 有大量气泡 | 无气泡 | _____ |
(讨论交流)为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与盐酸反应。
(反思评价)在该实验中要求金属要相同粗细,稀盐酸要_____;
且需将金属进行打磨,打磨的目的是_____。
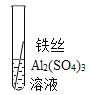
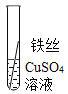
(实验验证)为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
操作 |
|
| 根据现象得出金属活动性顺序 |
现象 | 无明显现象 | _____。 | Al>Fe>Cu |
写出铁与硫酸铜溶液反应的化学方程式_____。
(拓展迁移)
(1)实验结束后,老师归纳总结了验证铁、铝、铜这三种金属的活动性顺序的两种方法。晓华提出还有别的方法也可以验证铁、铝、铜这三种金属的活动性顺序。她分别将铝丝和铜丝插入_____溶液中(填化学式),观察现象,即可知铁、铝、铜,这三种金属的活动性顺序。晓华的想法得到了大家一致赞同。
(2)除了用上述方法验证金属的活动性顺序,还可以依据_____做出判断。