ƒøƒ⁄»›
°æƒø°ø‘⁄“ª…’±≠÷– ¢”–22.3g Na2CO3∫ÕNaCl◊È≥…µƒπÃêÏ∫œŒÔ£¨º”143.1gÀÆ»‹Ω‚£¨÷∆≥…»‹“∫£ÆœÚ∆‰÷–÷Ω•µŒº”»‹÷ ÷ ¡ø∑÷ ˝Œ™10%µƒœ°—ŒÀ·£¨∑≈≥ˆ∆¯Ãµƒ◊‹÷ ¡ø”ÎÀ˘µŒ»Îœ°—ŒÀ·µƒ÷ ¡øπÿœµ«˙œfl»ÁÕºÀ˘ æ£∫ «Î∏˘æ›Ã‚“‚ªÿ¥Œ £∫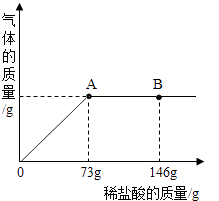
£®1£©µ±µŒº”¡À73gœ°—ŒÀ· ±£¨ ‘Õ®π˝º∆À„«Û≥ˆ∑≈≥ˆ∆¯Ãµƒ◊‹÷ ¡øŒ™g£Æ
£®2£©µ±µŒº”œ°—ŒÀ·÷¡Õº÷–Bµ„ ±£¨…’±≠÷–»‹“∫¿Ôµƒ»‹÷ «£®–¥ªØ—ß Ω£© £Æ
£®3£©µ±µŒº”¡À73gœ°—ŒÀ· ±£®º¥Aµ„ ±£©£¨…’±≠÷–Œ™≤ª±•∫Õ»‹“∫£¨ ‘Õ®π˝º∆À„«Û≥ˆ∆‰÷–∫¨»‹÷ µƒ÷ ¡øg£Æ
°æ¥∞∏°ø
£®1£©4.4
£®2£©NaCl∫ÕHCl
£®3£©23.4
°æΩ‚Œˆ°øΩ‚£ª£®1£©…Ë∑≈≥ˆ∆¯Ãµƒ◊‹÷ ¡øŒ™z£¨
Na2CO3+ | 2HCl®T2NaCl+H2O+ | CO2°¸ |
73 | 44 | |
73g°¡10% | z |
°‡ ![]() =
= ![]()
Ω‚÷Ƶ√£∫z=4.4g
À˘“‘¥∞∏ «£∫4.4£Æ£®2£©”…Õº æø…÷™£¨µ±µŒº”œ°—ŒÀ·÷¡Õº÷–Aµ„ ±£¨“— «ÕÍ»´∑¥”¶£¨‘ŸµŒº”œ°—ŒÀ·÷¡Õº÷–Bµ„ ±£¨—ŒÀ·æÕ”– £”‡£Æ
À˘“‘¥∞∏ «£∫NaCl∫ÕHCl£Æ£®3£©Ω‚£∫…Ë∑¥”¶∫Û…˙≥…NaClµƒ÷ ¡øŒ™x£¨ªÏ∫œŒÔ÷–Na2CO3µƒ÷ ¡øŒ™y£Æ
Na2CO3+ | 2HCl = | 2NaCl+H2O+CO2°¸ |
106 | 73 | 117 |
y | 73g°¡10% | x |
![]() =
= ![]() £¨
£¨ ![]()
Ω‚÷Ƶ√£∫y=10.6g£¨x=11.7g£¨
∑¥”¶∫Û»‹÷ NaClµƒ÷ ¡ø=11.7g+22.3g©Å10.6g=23.4g£Æ
À˘“‘¥∞∏ «£∫23.4g£Æ
°æøºµ„æ´Œˆ°ø’∆Œ’∏˘æ›ªØ—ß∑¥”¶∑Ω≥Ã Ωµƒº∆À„ «Ω‚¥±æµƒ∏˘±æ£¨–Ë“™÷™µ¿∏˜ŒÔ÷ º‰÷ ¡ø±»=œµ ˝°¡œ‡∂‘∑÷◊”÷ ¡ø÷Ʊ»£Æ

 ‘ƒ∂¡øÏ≥µœµ¡–¥∞∏
‘ƒ∂¡øÏ≥µœµ¡–¥∞∏°æƒø°øÕ¨—ß√«‘⁄ µ—È “∑¢œ÷”–“ª∆ø ¢”–Œfi…´»‹“∫µƒ ‘º¡∆ø£¨∆‰±Í«©∆∆À£¨¥”≤–”‡≤ø∑÷£®»ÁÕº£©Œfi∑®±Ê»œæflà« ≤√¥ŒÔ÷ µƒ»‹“∫£¨÷ªƒ‹ø¥≥ˆ»‹÷ µƒ÷ ¡ø∑÷ ˝Œ™10%£¨æ≠—ØŒ ¿œ ¶÷™µ¿ø…ƒ‹ ««‚—ıªØƒ∆°¢¬»ªØƒ∆°¢«‚—ıªØ∏∆ªÚúÀ·ƒ∆»‹“∫÷–µƒ“ª÷÷£ÆŒ™ÃΩæø∆‰≥…∑÷£¨ªØ—ß–À»§–°◊ȵƒÕ¨—ßΩ¯––»Áœ¬ÃΩæø£¨«Îƒ„π≤Õ¨≤Œ”Σ∫
£®1£©°æ≤È‘ƒ◊ ¡œ°ø–°◊ÈÕ¨—ß≤È‘ƒ¡Àœ‡πÿ◊ ¡œ£¨µ√÷™Àƒ÷÷ŒÔ÷ ‘⁄≥£Œ¬œ¬µƒ»‹Ω‚∂»»Áœ¬±ÌÀ˘ æ£∫
«‚—ıªØƒ∆ | ¬»ªØƒ∆ | «‚—ıªØ∏∆ | úÀ·ƒ∆ | |
»‹Ω‚∂»/g£®20°Ê£© | 51 | 36 | 0.16 | 21.5 |
°æÃ÷¬€∑÷Œˆ°ø–°◊ÈÕ¨—ßæ≠π˝Ã÷¬€£¨»œŒ™∏√»‹“∫≤ªø…ƒ‹ «»‹“∫£Æ
°æ µ—ȅ˺∆”ÎÃΩæø°ø
»°…Ÿ¡ø—˘∆∑»‹“∫”⁄ ‘π‹÷–£¨Õ˘∆‰÷–µŒº”∑”Ù ‘“∫£¨∑¢œ÷ ‘“∫±‰∫Ï…´£¨‘Ú∏√»‹“∫≤ªø…ƒ‹ «»‹“∫£Æ
£®2£©Œ™¡ÀΩ¯“ª≤Ω»∑∂®∏√»‹“∫µƒ≥…∑÷£¨–À»§–°◊ȵƒÕ¨—߅˺∆“‘œ¬ µ—È∑Ω∞∏ºÃ–¯Ω¯––ÃΩæø£¨«Îƒ„∞Ô√¶ÕÍ…∆ µ—È≤Ÿ◊˜º∞≤Ω÷Ë£Æ
µ—È≤Ÿ◊˜º∞≤Ω÷Ë | µ—Èœ÷œÛ | µ—ÈΩ·¬€ |
»°…Ÿ¡ø—˘∆∑»‹“∫”⁄ ‘π‹÷–£¨µŒº”¬»ªØ∏∆»‹“∫ | ”–∞◊…´≥¡µÌ≤˙…˙ | ∏√»‹“∫ «ÃºÀ·ƒ∆»‹“∫ |
»°…Ÿ¡ø—˘∆∑»‹“∫”⁄ ‘π‹÷–£¨µŒº” | ”–∆¯≈›≤˙…˙ |
°æ µ—È∑¥Àº°ø
–°◊ÈÕ¨—ßÃ÷¬€∫Û»œŒ™ªπø…“‘Õ®π˝Õ˘—˘∆∑»‹“∫÷–µŒº”≥Œ«Â ت“ÀÆ¿¥»∑∂®∏√»‹“∫µƒ≥…∑÷£¨«Î–¥≥ˆ∑¥”¶µƒªØ—ß∑Ω≥Ã Ω £Æ 
°æƒø°øƒ≥–£ªØ—ß–À»§–°◊ȵƒÕ¨—߅˺∆¡À»ÁÕºÀ˘ 浃ºÚ“◊√ª∆˜£¨À˚√«∂‘∑¥”¶∫Û∑œ“∫µƒ≥…∑÷’πø™¡ÀÃΩæø£∫ 
÷≥ˆŒ £∫∑¥”¶∫Ûµƒ∑œ“∫÷–∫¨”–ƒƒ–©≥…∑÷£ø
≤¬œÎ”Î µ—È£∫Õº““÷–∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™ £¨ ”…¥ÀÕ∆≥ˆ∑œ“∫÷–“ª∂®∫¨”–¬»ªØƒ∆»‹“∫£¨ø…ƒ‹∫¨”–úÀ·ƒ∆»‹“∫ªÚ—ŒÀ·£Æ
µ—È“ª£∫»∑∂®∏√∑œ“∫÷– «∑Ò∫¨”–—ŒÀ·
¢Ÿ—°‘Ò ‘º¡£∫∏˘æ›—ŒÀ·µƒªØ—ß–‘÷ £¨Õ¨—ß√«—°‘Ò¡Àœ¬ÕºÀ˘ æŒÂ÷÷≤ªÕ¨¿‡±µƒŒÔ÷ £¨∆‰÷–£¨Xø…“‘ «£®ÃÓ“ª÷÷æflÃÂŒÔ÷ µƒ√˚≥∆ªÚªØ—ß Ω£©£Æ
¢⁄ µ—È—È÷§£∫ƒ≥Õ¨—ß»°…Ÿ¡ø∑œ“∫”⁄ ‘π‹÷–£¨œÚ∆‰÷–º”»Î…Ÿ¡ø–ø¡££¨π€≤쵽 £¨ »∑∂®∑œ“∫÷–“ª∂®≤ª∫¨”–—ŒÀ·£Æ
µ—È∂˛£∫»∑∂®∑œ“∫÷– «∑Òªπ”–úÀ·ƒ∆
µ—È≤Ÿ◊˜ | œ÷œÛ | Ω·¬€ |
»°…Ÿ¡ø∑œ“∫”⁄ ‘π‹÷–£¨µŒº”…Ÿ | ∑œ“∫÷–∫¨”–úÀ·ƒ∆ |
µ—È»˝£∫¥¶¿Ì∑œ“∫£¨ªÿ ’¬»ªØƒ∆
”˚¥”∑œ“∫÷–µ√µΩ¥ø檵ƒ¬»ªØƒ∆£¨œÚ∑œ“∫÷–º”»Îπ˝¡øµƒ £¨ ‘Ÿæ≠π˝’Ù∑¢Ω·æߺ¥ø…µ√µΩ¥ø檵ƒ¬»ªØƒ∆æßãÆ