题目内容
【题目】密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如下图所示。下列说法正确的是
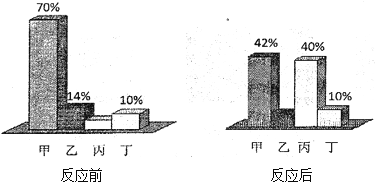
A. 该反应属于分解反应
B. 丁一定是该反应的催化剂
C. 反应前甲、乙的质量之和一定等于生成丙质量
D. 若消耗3g乙,则生成17g丙
【答案】D
【解析】根据质量守恒定律可知化学反应前面物质的总质量不变,故物质质量分数的变化即是物质质量的变化。由图可知,反应前甲为70g,反应后为42g,质量减少了28g,故是反应物;丁反应前为10g,反应后仍为10g,质量不变,可能没有参与反应,也可能是该反应的催化剂;乙反应前为14g,通过计算可知反应后为8g,质量减少了6g,故是反应物;计算可知丙反应前为6g,反应后为40g,质量增加了34g,属生成物。A、由质量关系该反应表示为:甲+乙→丙,属化合反应,错误;B、丁反应前为10g,反应后仍为10g,质量不变,可能没有参与反应,也可能是该反应的催化剂,错误;C、参加反应的甲、乙的质量之和一定等于生成丙质量,错误;D、乙和丙反应的质量比为6:34=3:17,故若消耗3g乙,则生成17g丙,正确。故选D。

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
【题目】在一个密闭容器内有M、N、X、Y四种物质,在一定条件下反应一段时间后,测得反应前后各物质量如下:
物质 | M | N | X | Y |
反应前质量/g | 8 | 11 | 18 | 10 |
反应后质量/g | 8 | 33 | 4 | 2 |
下列能正确表示容器中化学变化的表达式是( )
A. X+Y=M+N B. X+Y=N C. N=M+X+Y D. X+Y+M=N