题目内容
【题目】下图中A为一种混合气体,经分析已知只含两种元素,根据图中的转化关系:
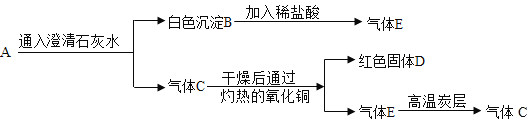
(1)写出上图物质的化学式:B________;C________;D________;E________。
(2)写出下列转化的化学方程式:C→D+E:_______。
【答案】CaCO3 CO Cu CO2 ![]()
【解析】
A中的气体通入澄清石灰水产生白色沉淀,则A中含有二氧化碳,白色沉淀B为碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,所以气体E为二氧化碳;气体C可以与氧化铜反应生成红色固体和另一种气体,说明气体C是具有还原性的气体,由于原混合气体中只含有两种元素,所以气体C是一氧化碳;一氧化碳和氧化铜在加热的条件下反应生成铜和二氧化碳,二氧化碳和碳在高温的条件下反应生成一氧化碳,所以红色固体D为铜。
(1)由分析可知:B是CaCO3,C是CO,D是Cu,E是CO2;
(2)一氧化碳和氧化铜在加热条件下生成二氧化碳和铜,化学方程式为:![]() 。
。

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
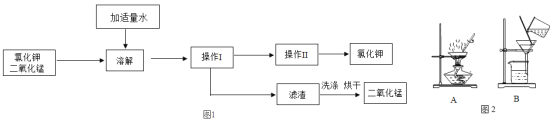
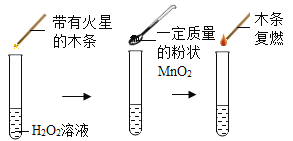
【题目】为探究催化剂对双氧水(H2O2)分解的催化效果,某研究小组做了如下实验:
实验一:
实验二:数据记录表
1%H2O2溶液(mL) | 50 | 50 | 50 |
加入MnO2的质量(g) | 0.1 | 0.2 | 0.4 |
测量40秒末得到O2体积(mL) |
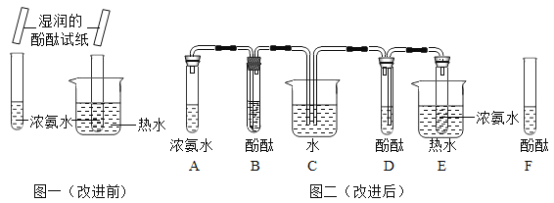
(实验一):图中的实验_____(填“能”或(不能))证明二氧化锰(MnO2)是过氧化氢分解反应的催化剂?理由_____。
(实验二):从表格的设计可以看出,该实验的目的是_____。所得氧气的体积分数越大,说明反应速率越_____(填“快”或“慢”)。