题目内容
【题目】铝、铁、铜是我们生活中常见的金属.
(1)铝制品具有很好的抗腐蚀性能,是因为铝在空气中其表面易形成致密的薄膜;
(2)图中发生反应后能生成色固体,做该实验时,在集气瓶中预先加入少量水可以防止; 
(3)生活中常作“双吸剂”的物质是 .
【答案】
(1)氧化铝
(2)黑;集气瓶破裂
(3)铁粉
【解析】解:(1)根据铝的化学性质,在常温下,铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化,从而使铝有较好的抗腐蚀性;(2)根据铁丝在氧气中剧烈燃烧,火星四射,生成黑色的四氧化三铁的现象解答,做该实验时,在集气瓶中预先加入少量水可以防止生成物溶化后溅落下来炸裂瓶底;(3)铁粉能与水和氧气同时反应,故常用于食品保鲜,故填:能与水和氧气反应.故答案为:(1)氧化铝(或三氧化二铝或Al2O3或氧化物)(2)黑;集气瓶破裂;(3)铁粉.
根据在常温下铝与空气氧气反应,铁丝在氧气中燃烧实验及现象进行分析解答本题.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),为确认其中的溶质,同学们进行了如下的探究活动.请你参与到其中去,回答有关问题. 
【进行猜想】猜想Ⅰ:该溶液的溶质是NaCl;
猜想Ⅱ:该溶液的溶质是NaOH;
猜想Ⅲ:该溶液的溶质是Na2CO3;
猜想 IV:该溶液的溶质是NaHCO3 .
【查阅资料】常温下物质的相关信息如表:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下稀溶液的pH | 7 | 13 | 11 | 9 |
(1)从物质的相关信息可知,该溶液的溶质不是NaHCO3 , 因为常温下NaHCO3溶液溶质的质量分数最大是(精确到01.%). 【进行实验】测定溶液的pH大于7,该溶液的溶质不是(填化学式).
(2)同学们又进行了如下实验,实验过程如图: 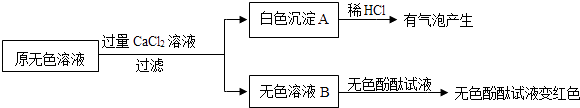
产生白色沉淀的化学方程式是 .
实验可以判断原无色溶液中含有的溶质有 .
【获得结论】
该瓶原来装的无色溶液的溶质是NaOH,并且(填“没有”、“部分”或“全部”)变质.
【拓展】
提纯该无色溶液的步骤是:先向无色溶液中加入适量的 , 然后过滤.反应化学方程式是 .
