题目内容
【题目】工业制取硝酸的流程如下:

(1)步骤①反应属于分解反应,其微观实质是_____ ; 步骤②是利用液态氮与液态氧的_____不同。
(2)步骤③中催化剂所起的作用是_____,相应的化学方程式为_____。
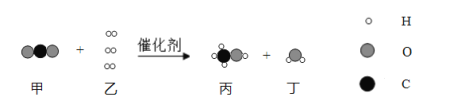
(3)步骤④的化学方程式是![]() ,则X的化学式为_____。
,则X的化学式为_____。
(4)流程中循环使用的物质是_____ (写化学式)。
【答案】水分子分为氢原子和氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子 沸点 催化作用  H2O NO
H2O NO
【解析】
(1)步骤①反应是水分解反应,微观实质是每一个水分子分为2个氢原子和1个氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子。步骤②是从液态空气中分离出氮气,是利用液态氮与液态氧的沸点不同。
(2)步骤③中催化剂所起的作用是催化作用,氮气和氢气在催化剂的作用下生成氨气,该反应的化学方程式为 。
。
(3)根据质量守恒定律,反应中原子的种类和数目不变,在化学方程式![]() 中,从微观上分析,反应前后N原子个数相等,反应后氢原子个数少了12个,氧原子个数少了6个,则X中只含氢原子和氧原子,且氢原子与氧原子个数比为2:1,所以X的化学式为H2O。
中,从微观上分析,反应前后N原子个数相等,反应后氢原子个数少了12个,氧原子个数少了6个,则X中只含氢原子和氧原子,且氢原子与氧原子个数比为2:1,所以X的化学式为H2O。
(4)NO与氧气反应生成二氧化氮,二氧化氮和水生成硝酸和一氧化氮,因此,流程中循环使用的物质是NO。

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目