题目内容
【题目】(1)一些物质在生活中有重要的用途。现有A 二氧化碳 B 活性炭 C 氮气 D 熟石灰 E 硝酸钾 F 不锈钢,选择适当的物质填空(填序号)。
①可用于冰箱除味剂的是____;
②参与绿色植物光合作用的是____;
③可用于制造炊具的是____;
④可充入食品包装袋中以防腐的是____;
⑤属于复合肥科的是____;
⑥可用于配制波尔多液的是_____。
(2)能源、材料和安全是人们关注的热点话题。请回答:
①太阳能电池路灯被越来越广泛地应用。如图标示的路灯各主要部件中,属于有机合成材料的是_____(填序号)。
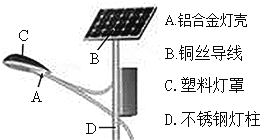
②固体叠氮化钠(NaN3)被广泛应用于汽车安全气囊,撞击后30毫秒内,叠氮化钠迅速分解生成两种单质。写出该反应的化学方程式_____。
【答案】B A F C E D C 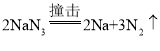
【解析】
(1)①活性炭具有吸附性,可以吸附色素和异味,故可用于冰箱除异味的是活性炭,故选B;
②二氧化碳是绿色植物进行光合作用的主要原料,故选A;
③不锈钢属于合金,抗腐蚀性好,具有导热性,可用于制作炊具,故选F;
④氮气的化学性质比较稳定,可充入食品包装袋中以防腐,故选C;
⑤硝酸钾含钾、氮两种营养元素,属于复合肥,故选E;
⑥熟石灰和硫酸铜可用于配制农药波尔多液,故选D;
(2)①A、铝合金属于合金,合金属于金属材料,不符合题意;
B、铜属于金属材料,不符合题意;
C、塑料属于三大合成材料之一,符合题意;
D、不锈钢属于合金,合金属于金属材料,不符合题意。
故选C;
②固体叠氮化钠(NaN3)被广泛应用于汽车安全气囊,撞击后30毫秒内,叠氮化钠迅速分解生成两种单质,根据质量守恒定律,化学反应前后,元素的种类不变,反应物中含Na、N,故生成物中也应含Na、N,故生成的两种单质是钠和氮气,该反应的化学方程式为: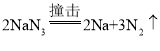 。
。

 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案【题目】Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取10g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
第1次 | 10 | m |
第2次 | 10 | 7.4 |
第3次 | 10 | 6.1 |
第4次 | 10 | 5.6 |
第5次 | 10 | n |
试回答下列问题:
(1)从以上数据可知,最后剩余的5.6g固体的成分是_____;表格中,m=_____,n=_____。
(2)黄铜样品中锌的质量分数为_____。
(3)计算所用稀硫酸中硫酸的质量分数为_____。