题目内容
 32、根据不同种金属与同种酸能否反应以及反应的剧烈程度,可判断金属的活动性.也可根据同种金属与不同种酸反应的快慢,来判断不同种酸的酸性强弱.为比较盐酸和醋酸的酸性强弱,设计了如下实验方案.装置如图所示(夹持和固定装置已略去).在两试管中分别加入过量镁条,同时将相同浓度的稀盐酸和稀醋酸注入相应试管中,观察产生氢气的速率和体积.
32、根据不同种金属与同种酸能否反应以及反应的剧烈程度,可判断金属的活动性.也可根据同种金属与不同种酸反应的快慢,来判断不同种酸的酸性强弱.为比较盐酸和醋酸的酸性强弱,设计了如下实验方案.装置如图所示(夹持和固定装置已略去).在两试管中分别加入过量镁条,同时将相同浓度的稀盐酸和稀醋酸注入相应试管中,观察产生氢气的速率和体积.试回答下列问题:
(1)盐酸与镁反应的化学方程式为
Mg+2HCl=MgCl2+H2↑
,反应的基本类型为置换
.(2)实验中收集到氢气的体积与时间的关系如图所示.分析图中曲线变化规律,可得出盐酸酸性比醋酸(填“强”或“弱”)
强
.
(3)实验中稀盐酸与镁条反应时,量筒中收集到氢气的体积比理论值高,可能的原因是
①④
.①反应放热 ②试管中有氢气残留
③实验装置气密性不好 ④酸液进入试管,占据了一定的体积.
分析:(1)根据金属与酸反应的规律书写化学方程式并判断反应类型;
(2)酸性越强,与金属反应速率越快;
(3)金属和酸放出热量,使气体体积膨胀,酸液从注射器试管,占据了一部分体积.
(2)酸性越强,与金属反应速率越快;
(3)金属和酸放出热量,使气体体积膨胀,酸液从注射器试管,占据了一部分体积.
解答:解:(1)盐酸与镁反应的化学方程式为 Mg+2HCl=MgCl2+H2↑,反应的基本类型为 置换.
(2)从图中看出,盐酸与镁反应生成氢气是速率快,说明盐酸酸性比醋酸强;
(3)实验中稀盐酸与镁条反应时,量筒中收集到氢气的体积比理论值高,就要从造成气体体积增大的原因考虑,如气体受热膨胀,进入的液体占据一部分体积等.
故答案为:(1)Mg+2HCl=MgCl2+H2↑;置换
(2)强
(3)①④
(2)从图中看出,盐酸与镁反应生成氢气是速率快,说明盐酸酸性比醋酸强;
(3)实验中稀盐酸与镁条反应时,量筒中收集到氢气的体积比理论值高,就要从造成气体体积增大的原因考虑,如气体受热膨胀,进入的液体占据一部分体积等.
故答案为:(1)Mg+2HCl=MgCl2+H2↑;置换
(2)强
(3)①④
点评:同种酸与不同中金属反应时,金属越活泼,反应速率越快,同样,同种金属与酸反应时,酸性强的酸反应速率快.

练习册系列答案
相关题目




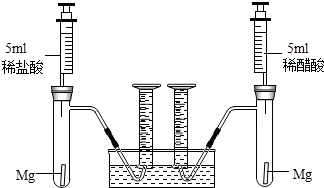 根据不同种金属与同种酸能否反应以及反应的剧烈程度,可判断金属的活动性.也可根据同种金属与不同种酸反应的快慢,来判断不同种酸的酸性强弱.为比较盐酸和醋酸的酸性强弱,设计了如下实验方案.装置如图所示(夹持和固定装置已略去).在两试管中分别加入过量镁条,同时将相同浓度的稀盐酸和稀醋酸注入相应试管中,观察产生氢气的速率和体积.
根据不同种金属与同种酸能否反应以及反应的剧烈程度,可判断金属的活动性.也可根据同种金属与不同种酸反应的快慢,来判断不同种酸的酸性强弱.为比较盐酸和醋酸的酸性强弱,设计了如下实验方案.装置如图所示(夹持和固定装置已略去).在两试管中分别加入过量镁条,同时将相同浓度的稀盐酸和稀醋酸注入相应试管中,观察产生氢气的速率和体积.

