题目内容
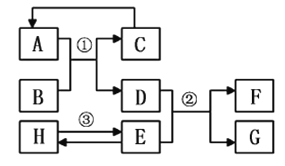
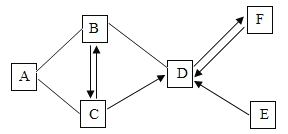
【题目】下图为实验室中常用装置。

请回答下列问题:
(1)标号为a的仪器名称是____________。
(2)实验室高锰酸钾制取较纯净的氧气,选择的发生装置和收集装置是_______________________。
(3)实验室用A、C装置组合制取某气体,写出其反应的化学方程式______________________________。
(4)用F装置除去二氧化碳气体中少量水蒸气,F中应放入试剂名称是____________。
【答案】长颈漏斗 BE ![]() 浓硫酸
浓硫酸
【解析】
(1)标号为a的仪器名称是长颈漏斗;
(2)实验室高锰酸钾制取较纯净的氧气,是加热固体制取气体,选择的发生装置B,氧气的密度比空气的大,可用向上排空气法收集,氧气难溶于水,可用排水法收集,其中排水法收集的气体较纯净,收集装置是E;
(3)实验室用A、C装置组合制取某气体,说明反应是固体和液体常温下反应,制取的气体密度比空气的小,可以是制取氢气,其反应的化学方程式![]() ;
;
(4)浓硫酸是常用的气体干燥剂,可干燥氨气外的常见气体,用F装置除去二氧化碳气体中少量水蒸气,F中应放入试剂名称是浓硫酸。

 优学名师名题系列答案
优学名师名题系列答案【题目】实验设计是化学实验的重要环节.请根据下列实验要求回答相关问题:
方案一:如图1所示
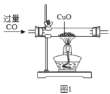
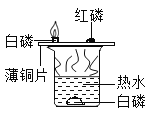
(1)请写出硬质玻璃管中发生反应的化学方程式_______;
(2)该实验能获得二氧化碳和一氧化碳混合气体,其原因是______;
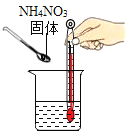
方案二:根据如图2装置所示请回答下列问题:(提示:饱和NaHCO3溶液的作用是除去HCl气体,部分夹持装置及导管已略去)
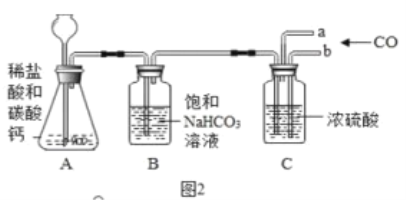
(1)写出装置A中发生反应的化学方程式_______;
(2)CO气体应由______(填a“或“b)通入,在C中混合后,由另一导管导出.
(3)装置C中浓硫酸的两点主要作用:①干燥气体,减少实验误差;②________
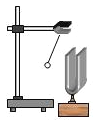
方案三:测定某钙片(主要成分CaCO3)中碳酸钙的质量分数,用如图3装置进行如下实验:
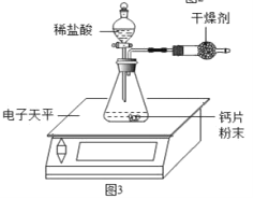
①取研碎后的钙片4克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入过量的稀盐酸,置于电子天平上测出装置总质量.
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.
③整理相关数据如下表
反应前总质量(克) | 275.58 |
反应后总质量(克) | 274.92 |
(1)小明结合表中数据.计算该钙片中碳酸钙的质量分数.(其它成分不与盐酸反应).______
(2)该实验中,如果装置中不加固态干燥剂(干燥剂的作用:吸水但不吸二氧化碳),则最终所算得钙片中碳酸钙的质量将_____(填偏大“偏小“不变”).