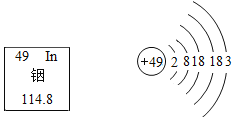题目内容
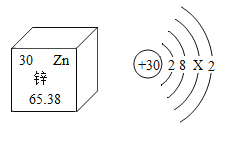
【题目】根据图回答下列问题:
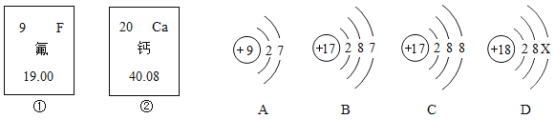

(1)很多科学家对元素周期表的发现和完善作出了重大贡献,写出其中一位科学家的名字___。X与Y在同一周期的原因是_________。
(2)钙元素的相对原子质量为________。
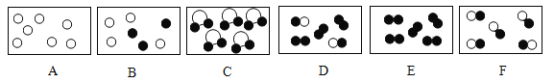
(3)A.B.C.D属于同种元素的粒子是______(填序号);达到稳定结构的是______.
(4)A粒子的化学性质与B.C.D中哪一种粒子的化学性质相似_______(填序号)
(5)锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示,则下列说法正确的是_____。
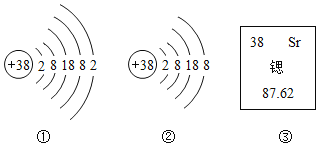
A①所表示的粒子在化学反应中容易失去电子
B从③可知该元素是金属元素
C②是锶离子结构示意图,符号为Sr2-
D锶元素在元素周期表中的第五周期
(6)请写出相应的化学符号
3个氟离子:_______,铵根离子________,氖气由_______构成,氯化钠由____构成。
(7)现有A、B、C、D四种元素,已知A元素原子核内只有一个质子,B元素是地壳中含量最多的元素,C元素的原子失去一个电子后和氖原子的核外电子排布相同,D元素的原子核外有三个电子层,第一层与第三层电子数之和比第二层多1个.则:试写出:A元素的符号为_____,B元素组成纯净物的化学式为____,C元素与D元素组成化合物的化学式是_____.
【答案】门捷列夫 原子的核外电子层数相同 40.08 BC CD B ABD 3F- NH4+ Ne Na+和Cl- H O2/O3 NaCl
【解析】
(1)门捷列夫发现了元素周期表;X和Y在同一周期是因为具有相同的电子层数,即原子的核外电子层数相同;
(2)从图②可知钙原子的相对原子质量为40.08;
(3)同种元素即原子核内质子数相同,A、B、C、D中只有B、C质子数相同;稳定结构是最外层电子数为8(第一层为2),所以B、C属于同种元素;CD两种粒子达到稳定结构;
(4)化学性质相似即最外层电子数相同,与A粒子最外层电子数相同的粒子为B;
(5)结合图中①、②、③可知:1.锶元素的元素符号为Sr,“锶”是金字旁,为金属元素;2.锶元素为第三十八号元素,核外有5个电子层;3.锶元素最外层电子数为2,小于4,容易失去2个电子,形成带正电荷的离子;4.相对原子质量为87.62。综合4条信息,A选项符合第3条,B选项符合第1条,D选项符合第2条,C选项锶元素形成的离子符号应为Sr2+,因此此空填ABD;
(6)3个氟离子的符号为“3F-”; 铵根离子的符号为“NH4+”;氖气是单原子分子,是由氖原子(Ne)构成的;氯化钠是由离子构成的物质,所含离子为“Na+”和“Cl-”;
(7)A元素原子核内只有一个质子,故A为H元素;B元素是地壳中含量最多的元素,故B为O元素;C元素的原子失去一个电子后和氖原子的核外电子排布相同,氖原子有时个电子,故C原子核外有10+1个电子,故C为Na元素;D元素的原子核外有三个电子层,第一层与第三层电子数之和比第二层多1个,第一层有2个电子,第二层8个,因此第三层电子个数为8+1-2=7,故D为Cl元素。故A的元素符号为H;由氧元素组成的纯净物为氧气(O2)或臭氧(O3);C为Na,D为Cl,组成的化合物为NaCl;
故答案为:门捷列夫;原子的核外电子层数相同;40.08;BC;C;B;ABD;3F-;NH4+;Ne;Na+和Cl-;H;O2/O3;NaCl。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案