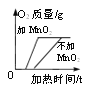
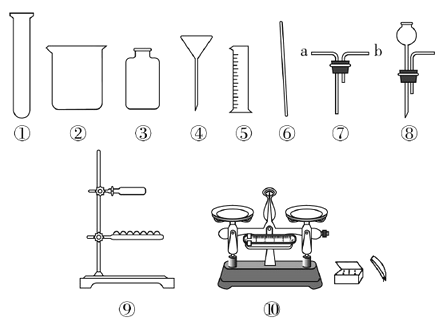
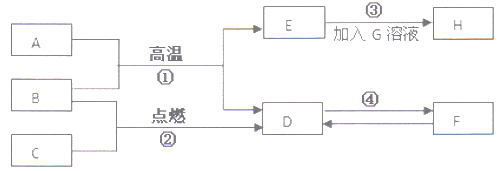
题目内容
【题目】下列是化学兴趣小组用过氧化氢制取氧气的实验,目的是探究影响化学反应快慢的因素,相关数据如下表所示(“常温”通常是指20℃;“浓度”指溶质的质量分数):
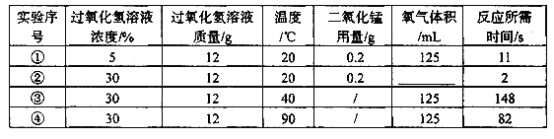
(1)表格中②的氧气体积为____mL,通过以上实验对比可知,化学反应快慢与温度的关系为___________。
(2)由上述实验可知,实验室用过氧化氢制取氧气最适合的条件是___________(填序号)。
(3)定量比较反应快慢,除了表格中的方法外,还可以采用______。写出该反应的化学方程式_____。
(4)如果要证明二氧化锰在化学反应前后的化学性质不变,可用什么实验方法?请写出实验的步骤、现象和结论_________。
(5)查阅资料可知:氧化铜也能加快过氧化氢的分解反应速率,给你一根铜丝、酒精灯、坩埚钳、石棉网、火柴、试管、5%过氧化氢溶液等。请你设计实验探究影响过氧化氢分解速率的因素,并写出实验步骤和实验现象。_________、_____________
【答案】 125; 在其它条件相同的前提下,温度越高反应速率越快(答案合理即可) ① 比较相同时问内收集的气体体积; 2H2O2 MnO2 2H2O+O2↑ 将反应后的溶液过滤得到黑色物质,放入试管中,再次加入过氧化氢溶液,观察有气泡产生,说明二氧化锰在化学反应前后化学性质不变 分别取等体积等浓度的过氧化氢溶液于两支试管中,取一根铜丝在酒精灯上加热至 黑色,插入其中的一支试管中,对比两支试管,观察产生气泡的速率。若放入铜丝的试管中产生的气泡较快,则说明氧化铜能加快过氧化氢分解的速率
【解析】(1) 根据控制变量法结合实验①②分析解答;根据对比实验③④分析解答;(2)根据实验时操作简便且制取气体易收集的原则分析解答;(3)根据可以比较相同时问内收集的气体体积解答;根据过氧化氢在二氧化锰的催化下分解生成水和氧气解答;(4) 要证明反应前后二氧化锰的质量的质量是否改变,则须称量反应前后二氧化锰的质量;证明其化学反应前后化学性质没有改变,可再取双氧水加入二氧化锰实验是否能生成氧气;(5) 根据催化剂能改变反应速率回答。(1) 根据控制变量法结合实验①②可知,表格中②的氧气体积为125mL,通过以上实验③④对比可知,化学反应快慢与温度的关系为在其它条件相同的前提下,温度越高反应速率越快;(2)实验室用过氧化氢制取氧气要求反应简便易操作,所以采用不加热而加催化剂的方法进行较合适,从易于收集的角度分析,反应的速度不能太快也不能太慢,所以最适合的条件是20℃时5%的过氧化氢溶液中加入少量二氧化锰,故选①;(3)定量比较反应快慢,除了表格中的方法外,还可以采用比较相同时问内收集的气体体积的方法;过氧化氢在二氧化锰的催化下分解生成水和氧气,反应的化学方程式为2H2O2MnO22H2O+O2↑;(4)要证明二氧化锰在化学反应前后的化学性质不变,可以将反应后的溶液过滤得到黑色物质,放入试管中,再次加入过氧化氢溶液,观察有气泡产生,说明二氧化锰在化学反应前后化学性质不变;(5) 要证明氧化铜能加快过氧化氢的分解,可以分别取等体积等浓度的过氧化氢溶液于两支试管中,取一根铜丝在酒精灯上加热至黑色,插入其中的一支试管中,对比两支试管,观察产生气泡的速率。若放入铜丝的试管中产生的气泡较快,则说明氧化铜能加快过氧化氢分解的速率。