题目内容
【题目】超氧化钾(KO2)是一种黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用它作制氧剂,供人们呼吸之用。化学方程式为: ![]() 。某学生为了验证这一实验并测定超氧化钾(KO2)样品中超氧化钾的质量分数(杂质既不挥发也不参与反应),先称取质量为m g的样品于装置D中,设计出如下实验装置进行实验。回答下列问题(已知KO2也能与水分反应,无水硫酸铜遇水分变蓝)。
。某学生为了验证这一实验并测定超氧化钾(KO2)样品中超氧化钾的质量分数(杂质既不挥发也不参与反应),先称取质量为m g的样品于装置D中,设计出如下实验装置进行实验。回答下列问题(已知KO2也能与水分反应,无水硫酸铜遇水分变蓝)。
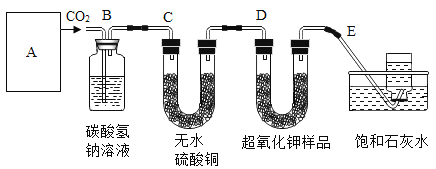
(1)A是实验室制取CO2的发生装置,其发生装置与实验室制取H2比的发生装置__________( 选填“相同”或“不相同”)
(2)B装置的作用是_________________。
(3)表明D中超氧化钾样品接近反应完毕时的现象是:_________________。
(4)反应结束后称取D中固体,其质量为ng,则样品中超氧化钾的质量分数为_________________。
(5)在A中有10.0克碳酸钙与足量盐酸完全反应后,如果生成的CO2全部被超氧化钾吸收,理论上D装置质量应减少0.4克,但实验上在实验后称量D装置,发现反应后其质量的变化量明显与理论值不符,可能原因可能是_____________(填序号)。
A 生成的CO2部分残留在A、B、C装置里未被D装置完全吸收
B D装置后面的水蒸气进入被超氧化钾吸收
C 超氧化钾不足量
D 装置B中反应生成的CO2也被D装置吸收
【答案】相同 吸收氯化氢气体 固体由黄色变成白色,水槽中的石灰水大量的变成浑浊 ![]() ABCD
ABCD
【解析】
(1)实验室制取二氧化碳,常用大理石或石灰石与盐酸反应,该反应的反应物是固体和液体,不需加热,属于固、液混合不加热型,实验室制取氢气是用锌与稀硫酸反应,反应的反应物是固体和液体,不需加热,属于固、液混合不加热型。A是实验室制取CO2的发生装置,其发生装置与实验室制取H2比的发生装置相同;
(2)碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,由于盐酸具有挥发性,制得的二氧化碳气体混有少量的氯化氢气体,氯化氢气体与形成盐酸。B装置的作用是吸收氯化氢气体;
(3)超氧化钾(KO2)是一种黄色固体,碳酸钾是一种白色固体。超氧化钾反应完毕会有大量的二氧化碳通入到石灰水中。表明D中超氧化钾样品接近反应完毕时的现象是固体由黄色变成白色,水槽中的石灰水大量的变成浑浊;
(4)设参加反应的超氧化钾的质量为x。
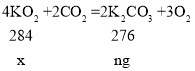
![]()
x=![]()
则样品中超氧化钾的质量分数=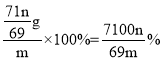 。
。
(5)在实验时称量D,发现反应后其质量该变量明显与理论值不符,是因为二氧化碳量的多少造成的,所以影响生成的二氧化碳气体的量的都会影响,故选AC;D装置后面的水蒸气进入被超氧化钾吸收,所以B正确;因为挥发的盐酸与碳酸氢钠反应生成的CO2也被D装置吸收,所以D也正确。故选ABCD。

 星级口算天天练系列答案
星级口算天天练系列答案【题目】微观示意图有助于我们认识化学物质和理解化学反应。已知甲和乙能在一定条件下反应生成丙和丁。
物质 | 甲 | 乙 | 丙 | 丁 |
|
微观示意图 |
|
|
|
|
(1)甲、乙、丙、丁中属于氧化物的是___(填序号)。
(2)在化学反应前后,可能变化的是__(填选项字母)。
A 原子种类B 原子数目 C 分子数目 D 元素种类
(3)丁物质过量排放可能引起的环境问题是___。
(4)该反应中,乙和丁的个数比为____。
【题目】某化学兴趣小组在老师的帮助下,开展了氢气的燃烧实验的相关探究:
(1)氢气燃烧的化学反应方程式为____________,在氢气点燃之前进行的操作是____________。
(2)作研究氢气的燃烧实验,需用试管收集不同体积比的氢气与空气的混合物,现用正确装置制取氢气,如何用试管(假设试管容积为10mL)收集氢气与空气体积比为4:1的混合气体,写出其操作方法:____________。
(3)用不同体积比的混合气体做氢气的燃烧实验,结果如表:
序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
氢气与空气体积比 | 9:1 | 8:2 | 7:3 | 5:5 | 3:7 | 1:9 | 0.5:9.5 |
点燃现象 | 安静燃烧 | 安静燃烧 | 弱的爆鸣声 | 强的爆鸣声 | 强的爆鸣声 | 弱的爆鸣声 | 不燃烧不爆鸣 |
分析上表信息,你对燃烧条件的新认识是可燃物能否燃烧除具备燃烧条件外,还与____________有关。