题目内容
配制溶质质量分数一定的氯化钠溶液常按以下操作顺序进行,请回答下列问题: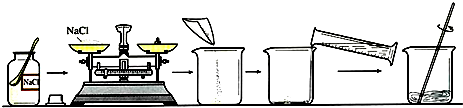
(1)配制100g10%的氯化钠溶液时,需要氯化钠 g,水 mL
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 .
A.增加适量氯化钠固体
B.减少适量氯化钠固体
C.添加砝码
D.调节平衡螺母
(3)称量时如果用质量为23.1g的烧杯盛放固体,在托盘天平上已放30g砝码,则天平上的游码位置应是下图中的 (填字母)
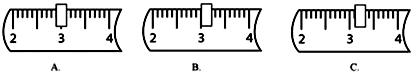
(4)下列仪器中,量取水时需要用到d和 (填序号),溶解时需要用到e和 (填序号)
a.烧杯 b.10mL量筒 c.100mL量筒 d.滴管 e.玻璃棒 f.药匙蒸发皿
将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是 .
(5)用量筒量取水时仰视读数,则配制的溶液中溶质质量分数
A.大于10% B.小于10%
C.等于10% D.无法确定.

(1)配制100g10%的氯化钠溶液时,需要氯化钠
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应
A.增加适量氯化钠固体
B.减少适量氯化钠固体
C.添加砝码
D.调节平衡螺母
(3)称量时如果用质量为23.1g的烧杯盛放固体,在托盘天平上已放30g砝码,则天平上的游码位置应是下图中的

(4)下列仪器中,量取水时需要用到d和
a.烧杯 b.10mL量筒 c.100mL量筒 d.滴管 e.玻璃棒 f.药匙蒸发皿
将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是
(5)用量筒量取水时仰视读数,则配制的溶液中溶质质量分数
A.大于10% B.小于10%
C.等于10% D.无法确定.
考点:一定溶质质量分数的溶液的配制,测量容器-量筒,称量器-托盘天平
专题:溶液、浊液与溶解度
分析:(1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量;
(2)使用托盘天平称量药品时应遵循“左物右码”,称量过程中他发现指针偏左了,说明药品质量大于砝码质量,应减少药品;
(3)应读游码左边的刻度;
(4)根据配制所用仪器及玻璃棒的作用来分析用途;
(5)根据量取水时是仰视读数,会导致水的体积偏大进行解答.
(2)使用托盘天平称量药品时应遵循“左物右码”,称量过程中他发现指针偏左了,说明药品质量大于砝码质量,应减少药品;
(3)应读游码左边的刻度;
(4)根据配制所用仪器及玻璃棒的作用来分析用途;
(5)根据量取水时是仰视读数,会导致水的体积偏大进行解答.
解答:解:(1)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为5%的氯化钠溶液,需氯化钠的质量=100g×10%=10g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-10g=90g,水的密度是1g/cm3,所以需要水的体积是90mL;
(2)用托盘天平称量NaCl时,步骤是:调节天平平衡,在右盘上加砝码和拨动游码,然后向左边托盘添加药品直至天平平衡;称量过程中他发现指针偏左了,说明NaCl的质量大于砝码质量,应减少NaCl;
(3)称量时如果用质量为23.1g的烧杯盛放固体,在托盘天平上已放30g砝码,则游码应拨到3.1g刻度出,且应读游码左边的刻度,故选C;
(4)配制溶液时,量取水时需要用到量筒和胶头滴管,溶解时用到烧杯和玻璃棒;溶解时用玻璃棒搅拌是为了加快氯化钠溶解速度;
(5)量取水时是仰视读数,会导致水的体积偏大,所以所配制的氯化钠溶液溶质质量分数会偏小;
故答案为:(1)10;90;(2)B;(3)C;(4)c;a;加速氯化钠溶解;(5)B.
(2)用托盘天平称量NaCl时,步骤是:调节天平平衡,在右盘上加砝码和拨动游码,然后向左边托盘添加药品直至天平平衡;称量过程中他发现指针偏左了,说明NaCl的质量大于砝码质量,应减少NaCl;
(3)称量时如果用质量为23.1g的烧杯盛放固体,在托盘天平上已放30g砝码,则游码应拨到3.1g刻度出,且应读游码左边的刻度,故选C;
(4)配制溶液时,量取水时需要用到量筒和胶头滴管,溶解时用到烧杯和玻璃棒;溶解时用玻璃棒搅拌是为了加快氯化钠溶解速度;
(5)量取水时是仰视读数,会导致水的体积偏大,所以所配制的氯化钠溶液溶质质量分数会偏小;
故答案为:(1)10;90;(2)B;(3)C;(4)c;a;加速氯化钠溶解;(5)B.
点评:本题难度不大,明确一定溶质质量分数溶液的配制的步骤、所需仪器、注意事项等是正确解答此类题的关键.

练习册系列答案
相关题目
正确的实验操作对实验结果、人身安全都非常重要.下列操作错误的是( )
A、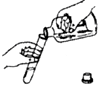 倾倒液体 |
B、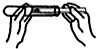 加入固体 |
C、 熄灭酒精灯 |
D、 加热液体 |
用I2O5可以测定空气受污染的程度,发生化学反应的化学方程式为:I2O5+5CO═I2+5CO2.根据生成CO2的多少,可以判断CO的含量.关于这个反应,下列说法正确的是( )
| A、参加反应的I2O5的质量等于生成物I2的质量 |
| B、反应物所含元素种类与生成物所含元素种类相同 |
| C、参加反应的I2O5和CO的质量比等于生成的 I2和CO2的质量比 |
| D、参加反应的I2O5中的氧原子总数等于生成物CO2中的氧原子总数 |
 为研究某含C、H、O元素的有机物的组成,将8.00g该有机物在氧气中充分燃烧,并将生成物全部通过如图的装置,测得下表的结果.(提示:氯化钙是干燥剂)
为研究某含C、H、O元素的有机物的组成,将8.00g该有机物在氧气中充分燃烧,并将生成物全部通过如图的装置,测得下表的结果.(提示:氯化钙是干燥剂) 在实验室里,可以用如图所示的装置制取铁,玻璃管内放的是氧化铁,请回答下列问题.
在实验室里,可以用如图所示的装置制取铁,玻璃管内放的是氧化铁,请回答下列问题.