题目内容
将下列物质分别按混合物、纯净物、单质、化合物分类正确的一组是①空气 ②氧气 ③水蒸气 ④高锰酸钾 ⑤铁粉 ⑥氮气( )| 混合物 | 纯净物 | 单质 | 化合物 | |
| ① | ①③ | ②⑤⑥ | ② | ④ |
| ② | ①②⑤⑥ | ③④ | ②⑤ | 3④ |
| ③ | ① | ②③④⑤⑥ | ②⑤⑥ | ③④ |
| ④ | ①③④ | ②⑤⑥ | 4 | 1④ |
A.①
B.②
C.③
D.④
解答:解:①空气中含有氧气、氮气、二氧化碳等物质,属于混合物;②氧气是由一种元素组成的单质;③水蒸气是由氢氧两元素组成的纯净物,属于化合物;④高锰酸钾是由钾、锰、氧三种元素组成的化合物;⑤铁粉是由铁元素组成的单质;⑥氮气是由氮元素组成的单质;故选C
点评:解答本题先分析物质是由几种物质组成的,如果只有一种物质组成就属于纯净物.然后根据物质的组成元素种类判断是单质还是化合物.

某学习小组对硫酸进行如下研究:
(1)已知相同温度下,硫酸的质量分数越大溶液的酸性越强。若对稀硫酸进行如下操作,溶液的pH因化学变化而升高的有 (填字母)。
A.加少量水 B.加少量铁粉 C.加少量氢氧化钾 D.加少量浓硫酸
| 时间/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水质量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
(2)向两个烧杯中分别注入硫酸甲(溶质质量分数为98%,密度为1.84g/cm3)和硫酸乙(硫酸甲与水的按体积比1︰1混和)各10mL,称量并记录不同时间(h)两种硫酸溶液吸水的质量,数据见下表:
①若量取硫酸甲时俯视读数,则所配硫酸乙的溶质质量分数将 (填填“偏大”、“偏小”或“不变”。
②由表中实验数据可知:有关硫酸吸水性的说法不正确的是 (填字母)。
A.硫酸甲和乙都有吸水性 B.只有硫酸甲有吸水性 C.硫酸甲的吸水性较硫酸乙强
(3)在高效复习课堂中,同学们利用稀释后的稀硫酸,硝酸钡、氢氧化钠、碳酸钾等物质的溶液对 “复分解反应发生的条件”进行再探究。
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中符合下列条件的两个化学方程式:
一个中和反应 ;一个有沉淀生成的反应 。
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液。经测定,该溶液显酸性。则在该溶液中一定含有的离子是 。为了验证该溶液中可能含有的阴离子是否存在,请按如下实验进行验证。
| 溶液中可能含有的离子 | 设计实验验证(实验步骤、现象及对应的结论) |
|
|
|
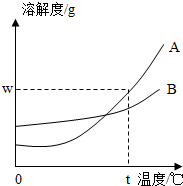 如图所示,A、B两种固体物质的溶解度曲线:
如图所示,A、B两种固体物质的溶解度曲线: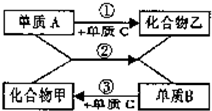
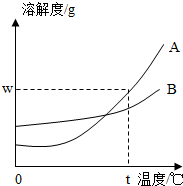 如图所示,A、B两种固体物质的溶解度曲线:
如图所示,A、B两种固体物质的溶解度曲线: