题目内容
【题目】氧化钙俗名生石灰,某同学针对氧化钙设计了如下实验方案,下列分析不正确的是( )
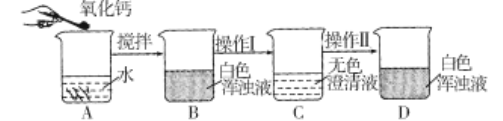
A.A 中发生反应的化学方程式为:CaO + H2O = Ca(OH)2
B.分离 B 中难溶物的操作I为过滤
C.可以选择稀盐酸或酚酞试液来证明 C 中不是水而是一种溶液
D.操作II 是加入某种物质使无色澄清液出现白色固体,如果加入的是饱和碳酸钠溶液,白色固体的化学式是 CaCO3;如果加入的是固体氢氧化钠(全部溶解),白色固体的化学式是 Ca(OH)2
【答案】C
【解析】
A、A 中发生的反应是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO + H2O = Ca(OH)2,故A正确;
B、过滤可以将固体与液体分离,所以分离B中难溶物的操作I为过滤,故B正确;
C、氢氧化钙与盐酸能反应但没有明显的实验现象,不能用盐酸证明 C 中不是水而是一种溶液,故C错误;
D、氢氧化钙和碳酸钠反应会生成碳酸钙沉淀和氢氧化钠,所以加入的是饱和碳酸钠溶液,白色固体的化学式是CaCO3,氢氧化钙的溶解度随温度的升高而减小,氢氧化钠固体溶于水放出热量,所以加入的是固体氢氧化钠(全部溶解),白色固体是析出的氢氧化钙,其化学式是Ca(OH)2,故D正确。故选C。

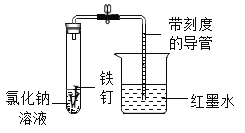
【题目】兴趣小组借助如图装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积百分数。
(1)实验前用砂纸打磨铁钉至光亮的目的是_____。
(2)铁生锈发生复杂的化学反应,首先是铁与氧气和水反应生成氢氧化亚铁,请写出该反应的化学反应方程式_____
(3)已知试管剩余空间和导管的体积为20mL,导管截面积约为1cm2,充分反应后,形成稳定液柱时,读取读数为4.1cm,则空气中氧气的体积分数为_____%(保留小数点后一位)。
(4)实验时发现上述测量过程因反应较慢耗时较长,现对影响铁生锈速率的因素作如下
(提出假设)假设一:溶液的酸碱度;
假设二:NaC1溶液的浓度;
请你再提出一种影响铁生锈快慢的因素,假设三:_____。
(实验探究)借助上述实验装置,通过控制铁钉用量等其他条件均相同时,调节溶液的pH获得了如表实验数据:
pH | 2.0 | 5.5 | 6.0 | 6.5 | 7.0 | 8.0 |
液柱高度(cm) | 0 | 0.6 | 4.1 | 4.1 | 4.1 | 4.1 |
形成稳定液柱时间(min) | 3.0 | 3.0 | 5.1 | 5.3 | 15.6 | 17.5 |
(实验结论)根据实验数据分析,为缩短实验测定时间,pH的最佳范围是_____;还可以采取何种方法进一步缩短实验时间_____(答一条即可)。
(实验反思)当pH=2时,没有观察到稳定液柱形成的原因是_____。