��Ŀ����
ij����С��Ԥ�ⶨ��ȸʯ�м�ʽ̼��ͭ[Cu2��OH��2CO3]�������������ֳ�ȡ30g�ÿ�ȸʯ��Ʒ�����ձ��У�����μ���ϡ������ǡ����ȫ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ��ͭCu2��OH��2CO3+4HCl=2CuCl2+CO2��+3H2O�������ĸ�ϡ����146g���������ʲ���ϡ���ᷴӦ��Ҳ������ˮ�������ճƵ��ձ���ʣ�����ʵ�����Ϊ171.6g������
��1����ȸʯ�м�ʽ̼��ͭ������������
��2��������Һ�����ʵ����������������������0.1%��
��������
�����������1�������⣬CO2������=30g+146g��171.6g=4.4g
���ȸʯ�м�ʽ̼��ͭ������Ϊx�������Ȼ�ͭ����Ϊy
Cu2��OH��2CO3+4HCl=2CuCl2+CO2��+3H2O
222 270 44
x y 4.4g
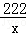 =
=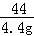 x=22.2g
x=22.2g
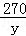 =
=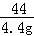 y=27g
y=27g
���ȸʯ�м�ʽ̼��ͭ����������Ϊ ��100%=74%
��100%=74%
��2�����ݣ�1���ļ����֪����Ӧ����Һ������=171.6g����30g��22.2g��=163.8g
��������Һ�����ʵ���������=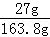 ��100%��16.5%
��100%��16.5%
�𣺿�ȸʯ�м�ʽ̼��ͭ����������Ϊ74%��������Һ�����ʵ���������Ϊ16.5%
���㣺���ݻ�ѧ��Ӧ����ʽ�ļ��㣻�й��������������ļ���

 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�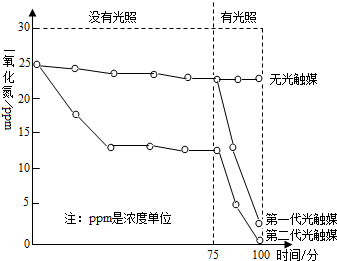 ��2012?���ݣ�����ij��˾���Ƴ���һ����ӱ�ġ�װ��������
��2012?���ݣ�����ij��˾���Ƴ���һ����ӱ�ġ�װ��������