题目内容
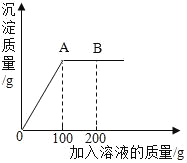
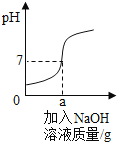
【题目】用溶质质量分数为5%的NaOH溶液中和73g的稀盐酸,反应过程中溶液的酸碱度变化如图所示。请计算:
(1)盐酸和NaOH反应的化学方程式是______
(2)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液100g,需要水________克。
(3)当a为80g时,所得溶液中溶质的质量分数是多少______(结果精确到0.1%)?
【答案】NaOH+HCl=NaCl+H2O 50 3.8%
【解析】
(1)盐酸和NaOH反应的生成氯化钠和水,故化学方程式是:NaOH+HCl=NaCl+H2O;故填:NaOH+HCl=NaCl+H2O
(2)设需要水的质量为x,根据溶质在稀释前后质量不变,![]() ;
;![]() ;故填:50
;故填:50
(3)设80gNaOH溶液中和73g的稀盐酸反应生成的氯化钠的质量为x。
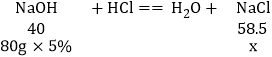
![]() ;
;![]() 。
。
反应后所得溶液中溶质的质量分数为![]()
答:当NaOH溶液为80g时,所得溶液中溶质的质量分数是3.8%。故填:3.8%

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目