题目内容
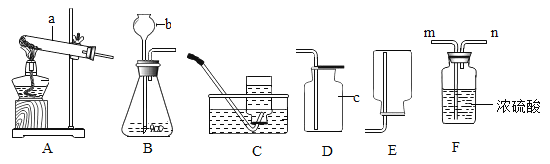
【题目】用如图装置测定空气中氧气的含量。

(1)红磷燃烧的符号表达式是______________。
(2)集气瓶中空气的体积为450 mL,量筒中水的体积为500 mL。能证明空气中氧气含量的现象是__________。
【答案】![]() 冷却至室温后,打开止水夹,量筒中的水进入集气瓶,集气瓶中液面上升,量筒中液面下降,最终量筒中剩余水的体积约为410 mL
冷却至室温后,打开止水夹,量筒中的水进入集气瓶,集气瓶中液面上升,量筒中液面下降,最终量筒中剩余水的体积约为410 mL
【解析】
(1)红磷燃烧,红磷与氧气在点燃条件下生成五氧化二磷,反应的符号表达式为
![]() ;
;
(2)集气瓶中红磷燃烧消耗了氧气,冷却至室温后,集气瓶内压强小于外界压强,打开止水夹,量筒中的水进入集气瓶,空气中氧气的体积分数约为五分之一,集气瓶中空气的体积为450 mL,氧气的体积约为![]() ,进入水的体积即为氧气的体积,量筒中水的体积为500 mL,最终量筒中剩余水的体积为
,进入水的体积即为氧气的体积,量筒中水的体积为500 mL,最终量筒中剩余水的体积为![]() ,因此能证明空气中氧气含量的现象是:冷却至室温后,打开止水夹,量筒中的水进入集气瓶,集气瓶中液面上升,量筒中液面下降,最终量筒中剩余水的体积约为410 mL。
,因此能证明空气中氧气含量的现象是:冷却至室温后,打开止水夹,量筒中的水进入集气瓶,集气瓶中液面上升,量筒中液面下降,最终量筒中剩余水的体积约为410 mL。

 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温是常指20℃)
实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰/g | 氧气/mL | 反应所需的时间/s |
a | 5 | 12 | 20 | 0.2 | 125 | 11 |
b | 30 | 12 | 20 | 0.2 | 125 | 2 |
c | 30 | 12 | 40 | 125 | 148 | |
d | 30 | 12 | 90 | 125 | 82 |
(1)通过验a和b对比可知,化学反应快慢与 __________________有关。
(2)通过对比实验____________可知化学反应快慢与温度有关,且表现为____________。
(3)写出实验室该实验的表达式__________________。
【题目】在测定空气中氧气含量的实验中,赵敏采用了如图所示装置:由两个注射器组成的密闭容器中留有25mL空气(不考虑玻璃管内气体的体积),给装有细铜丝的玻璃管加热,同时交替缓慢推动两个注射器的活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却后,将气体推至一个注射器内,观察密闭装置内空气体积的变化。
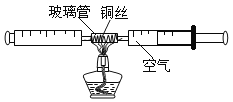
(资料)铜丝在加热时与空气中的氧气反应生成黑色的氧化铜固体。
(1)在加热过程中,交替缓慢推动两个注射器的活塞的目的是_____。
(2)写出该实验中反应的文字表达式:_____。
(3)赵敏测得实验结果如下:
反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
25mL | 21mL |
由此数据可以推算出她测定的空气中氧气的体积分数_____21%(填“>”“<”或“=”)。造成该实验出现误差的原因可能是_____(填序号,多选)
①装置气密性差
②读数时没有冷却至室温
③加入铜丝量太少
④加入铜丝量太多
【题目】水在生产、生活中有着及其重要的作用。
①15%的氯化钠溶液具有消毒作用,其中溶剂是______,配置100g该溶液,需要氯化钠______g。配置过程中会导致溶液质量分数偏大的可能原因是______(写出一条即可)。
②对氯化钠溶液进行焰色反应,火焰呈______色;滴加硝酸银溶液,观察到生成白色沉淀,请写出该反应的化学方程式______。
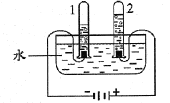
③下图电解水实验揭示了水的组成。实验中得到氢气的试管是______(选填“1”“2”)。反应的化学方程式为______。2mol水中约含_____个水分子。
④![]() 、
、![]() 、
、![]() 在不同溶剂中的溶解度如下表所示。
在不同溶剂中的溶解度如下表所示。
表1 ![]() 、
、![]() 、
、![]() 分别在水中的溶解度(g/100g水)
分别在水中的溶解度(g/100g水)
t/℃ |
|
|
|
0 | 42 | 7.1 | 35.7 |
10 | 51 | 122 | 35.8 |
20 | 109 | 21.8 | 36.0 |
30 | 119 | 39.7 | 36.3 |
|
|
| |
最多溶解的质量(g) | 17.3 | <0.01 | 0.1 |
根据表1和表2提供的数据回答下列问题
Ⅰ. ![]() 在水中的溶解度随温度升高而______(选填“增大”“减小”)。
在水中的溶解度随温度升高而______(选填“增大”“减小”)。
Ⅱ.20℃时,饱和食盐水中溶质质量分数为______。
Ⅲ.常温下,将![]() 通入饱和
通入饱和![]() 的乙醇溶液中,反应的方程式为______,可观察到的现象______。
的乙醇溶液中,反应的方程式为______,可观察到的现象______。