题目内容
将一定量的A、B、C、D四种物质置于一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如下表.下列说法中错误的是( )
|
分析:化学变化前后各物质的质量总和不变,利用质量守恒定律,计算出反应后B物质的质量;根据反应后质量增加的物质为生成物、质量减小的物质为反应物,判断反应的发生情况.
解答:解:A、根据质量守恒定律,反应后物质B的质量=(32+18+1+2)g-(26+2+12)g=13g.A、B的质量反应后减少,是反应物;C的质量反应后质量增加,是生成物;D的质量反应后不变,可能是催化剂,也可能不反应,故说法正确;
B、参加反应的A物质的质量=32g-12g=20g,参加反应C物质的质量=26g-1g=25g,反应中A、C的质量比=20g:25g=4:5,故说法正确.
C、根据质量守恒定律,反应后物质B的质量=(32+18+1+2)g-(26+2+12)g=13g,故说法错误;
D、A、B的质量反应后减少,是反应物;C的质量反应后质量增加,是生成物,故该反应是化合反应,C一定是化合物,故说法正确;
故选C.
B、参加反应的A物质的质量=32g-12g=20g,参加反应C物质的质量=26g-1g=25g,反应中A、C的质量比=20g:25g=4:5,故说法正确.
C、根据质量守恒定律,反应后物质B的质量=(32+18+1+2)g-(26+2+12)g=13g,故说法错误;
D、A、B的质量反应后减少,是反应物;C的质量反应后质量增加,是生成物,故该反应是化合反应,C一定是化合物,故说法正确;
故选C.
点评:该题要求学生要掌握好质量守恒定律并能灵活的加以运用,还要求学生具有会从图表中挖掘出有效数据进行处理的能力.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
将一定量的A、B、C、D四种物质放入一密闭容器中在一定条件下反应一段时间后,测得反应后各物质的质量如下:
|
将一定量的A、B、C、D四种物质置于一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如下表.下列说法中错误的是
| 物 质 | A | B | C | D |
| 反应前的质量/g | 32 | 18 | 1 | 2 |
| 反应后的质量/g | 12 | 待测 | 26 | 2 |
- A.A和B是反应物,D可能是催化剂
- B.反中A、C的质量比为4:5
- C.上表中的待测数据的数值为5
- D.该反应是化合反应,C一定是化合物
将一定量的A、B、C、D四种物质放入一密闭容器中在一定条件下反应一段时间后,测得反应后各物质的质量如下:
下列说法错误的是:( )
A.反应中A和B是反应物,D可能是催化剂
B.反应后A物质的质量为6.64g
C.C物质中元素的种类,一定等于A、B两种物质中元素的种类
D.若物质A与物质B的相对分子质量之比为2:1,则反应中A和B的化学计量数之比为2:1
| 物质 | A | B | C | D |
| 反应前质量∕g | 6.4 | 3.2 | 4.0 | 0.5 |
| 反应后质量∕g | 待测 | 2.56 | 7.2 | 0.5 |
A.反应中A和B是反应物,D可能是催化剂
B.反应后A物质的质量为6.64g
C.C物质中元素的种类,一定等于A、B两种物质中元素的种类
D.若物质A与物质B的相对分子质量之比为2:1,则反应中A和B的化学计量数之比为2:1
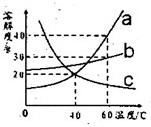 25、图中是物质a、b、c三种固体物质的溶解度曲线.试根据图象回答:
25、图中是物质a、b、c三种固体物质的溶解度曲线.试根据图象回答: