题目内容
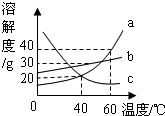
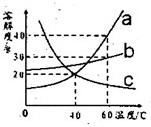 25、图中是物质a、b、c三种固体物质的溶解度曲线.试根据图象回答:
25、图中是物质a、b、c三种固体物质的溶解度曲线.试根据图象回答:(1)
40
℃时,a、c的溶解度相同;(2)60℃时,一定量的a、b分别溶解在100g水里达到饱和,冷却到40℃时,析出晶体较多的是
a
;(3)40℃时将a物质15g加入50克水中,所得溶液质量为
60
g;(4)40℃时a、b、c三物质的饱和溶液升温至60℃后,溶质质量分数从大到小顺序是
bac
;(5)欲使60℃时b的不饱和溶液变为饱和溶液,可采取的方法是
②③
;(选填:①升温 ②加b固体 ③蒸发溶剂)(6)为了从混有少量b的物质a中提取纯净的a,可采用
冷却热饱和溶液
的方法.分析:由溶解度曲线,可以查出a、c的溶解度相同的温度;由a、b两种物质的溶解度受温度的影响的变化趋势,可以判断降温后析出晶体的质量;由40℃时a的溶解度,可以判断形成溶液的质量;由在40℃时,三种物质的溶解度大小关系,可以确定三种物质的饱和溶液中溶质的质量分数;由三种物质的溶解度受温度的影响的变化趋势,可以判断升温时三种溶液的溶质质量分数由大到小的顺序.由b的溶解度受温度的影响变化趋势可以判断b的不饱和溶液变为饱和溶液采取的方法.由a的溶解度受温度的影响较大,可以确定提纯a采取的方法.
解答:解:(1)40℃时,a、c的溶解度曲线交于一点,故它们的溶解度相同;
(2)由于a的溶解度随着温度的升高而增大且受温度的影响变化最大,故60℃时,一定量的a、b的饱和溶液,冷却到40℃时,析出晶体较多的是a;
(3)40℃时a的溶解度为20g,将a物质15g加入50克水中,只能溶解10g,所得溶液质量为60g;
(4)根据三物质的溶解度曲线可知,在40℃时,三物质的溶解度大小关系是b>a=c,即在40℃时,三物质的饱和溶液中溶质的质量分数的大小关系是b>a=c;由于a和b的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,因此给它们的饱和溶液升温至60℃时,a和b的饱和溶液就会变成不饱和溶液,溶液中溶质的质量分数不变,c的饱和溶液中有晶体析出,溶液中溶质的质量分数就会减小,因此升温后溶液中溶质的质量分数大小关系为b>a>c.
(5)b的溶解度受温度的影响变化不大,故欲使60℃时b的不饱和溶液变为饱和溶液,可采取的方法是加b固体或蒸发溶剂的方法.
(6)a的溶解度受温度的影响较大,要从含有少量a的b溶液中得到较多的a晶体,通常可采用冷却热饱和溶液的方法.
故答案为:(1)40;(2)a;(3)60;(4)bac;(5)②③;(6)冷却热饱和溶液(或降温结晶或冷却结晶).
(2)由于a的溶解度随着温度的升高而增大且受温度的影响变化最大,故60℃时,一定量的a、b的饱和溶液,冷却到40℃时,析出晶体较多的是a;
(3)40℃时a的溶解度为20g,将a物质15g加入50克水中,只能溶解10g,所得溶液质量为60g;
(4)根据三物质的溶解度曲线可知,在40℃时,三物质的溶解度大小关系是b>a=c,即在40℃时,三物质的饱和溶液中溶质的质量分数的大小关系是b>a=c;由于a和b的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,因此给它们的饱和溶液升温至60℃时,a和b的饱和溶液就会变成不饱和溶液,溶液中溶质的质量分数不变,c的饱和溶液中有晶体析出,溶液中溶质的质量分数就会减小,因此升温后溶液中溶质的质量分数大小关系为b>a>c.
(5)b的溶解度受温度的影响变化不大,故欲使60℃时b的不饱和溶液变为饱和溶液,可采取的方法是加b固体或蒸发溶剂的方法.
(6)a的溶解度受温度的影响较大,要从含有少量a的b溶液中得到较多的a晶体,通常可采用冷却热饱和溶液的方法.
故答案为:(1)40;(2)a;(3)60;(4)bac;(5)②③;(6)冷却热饱和溶液(或降温结晶或冷却结晶).
点评:本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
 图中是物质a、b、c三种固体物质的溶解度曲线.试根据图象回答:
图中是物质a、b、c三种固体物质的溶解度曲线.试根据图象回答: