题目内容
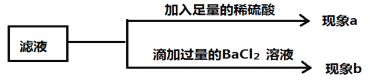
【题目】(6分)某化学兴趣小组同学取ag氯酸钾和2g二氧化锰加热制取氧气并进行如下操作。
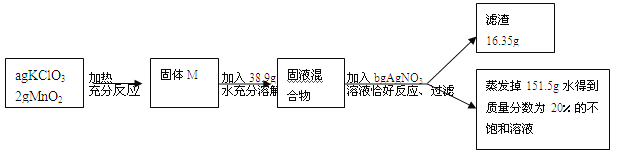
(1)滴加硝酸银溶液时发生反应的化学方程式为___________________________。
(2)固体M的成分______(填化学式);
(3)M中与硝酸银反应的物质的质量为X,列出求解x的比例式______;
(4)加入的氯酸钾质量为______
(5)加入硝酸银溶液质量分数为_______。
【答案】(1)KCl +AgNO3 ==AgCl↓ + KNO3(2)KCl ;MnO2(3)74.5:143.5=X :14.35克(4)12.25克(5)10%
【解析】
试题分析:氯酸钾在二氧化锰做催化剂的条件下加热分解生成氯化钾和氧气,所以M是混合物,其中有氯化钾和二氧化锰,所以滴加硝酸银溶液时发生反应的化学方程式为KCl +AgNO3 ==AgCl↓ + KNO3;滤渣中含有2克的二氧化锰,其余是氯化银沉淀,所以根据沉淀的质量可以根据化学方程式求得需要的结果;设需要氯化钾的质量为X,需要硝酸银的质量为Y,同时生成硝酸钾的质量为Z。
KCl +AgNO3 ==AgCl↓ + KNO3
74.5 170 143.5 101
X Y 14.35克 Z
列比例式得:74.5:X=170:Y=143.5:14.35克 =101:Z X=7.45克,Y=17克 Z=10.1克
设生成氯化钾的质量为7.45克需要氯酸钾的质量为X。
2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
245 149
X 7.45克 列比例式得: 245:X=149:7.45克 X=12.25克。
最终溶液的质量分数为20%,所以溶液得到质量=10.1/20%=50.5克,所以加入的硝酸银溶液的质量=50.5克+14.35克+151.5克-38.9克-7.45克=170克。所以加入硝酸银溶液质量分数为=17克/170克×100%=10%。