题目内容
【题目】现有四种含铁化合物:①FeO ②Fe2O3 ③Fe3O4 ④FeS,其含铁元素的质量分数由大到小的排列顺序为______________(填序号,下同);相同质量的①硫 ②磷 ③铁 ④镁分别在氧气中完全燃烧,消耗氧气的质量由小到大的排列序为_______________。
【答案】① ③ ② ④ ③ ④ ① ②
【解析】
比较四种铁化合物的含铁量的大小,通过计算铁元素质量分数进行比较;比较相同质量的①硫 ②磷 ③铁 ④镁分别在氧气中完全燃烧,消耗氧气的质量的大小,通过化学方程式进行计算比较。
(1)分别列出铁元素质量分数表达式,①为![]() 、 ②为
、 ②为![]() 、③为
、③为![]() 、④为
、④为![]() ,分别把四个表达式化简成分子相同的式子,
,分别把四个表达式化简成分子相同的式子,![]() 、
、![]() 、
、![]() 、
、![]() ,因为
,因为![]() >
>![]() >
>![]() >
>![]() ,所以四种含铁化合物:①FeO ②Fe2O3 ③Fe3O4 ④FeS,其含铁元素的质量分数由大到小的排列顺序为① ③ ② ④ 。
,所以四种含铁化合物:①FeO ②Fe2O3 ③Fe3O4 ④FeS,其含铁元素的质量分数由大到小的排列顺序为① ③ ② ④ 。
(2)写出①硫、 ②磷、 ③铁、 ④镁分别在氧气中完全燃烧的化学方程式: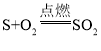 、
、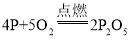 、
、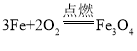 、
、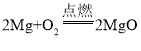 ,从方程式可知,四种物质与氧气的质量比并化简为
,从方程式可知,四种物质与氧气的质量比并化简为![]() 、
、![]() 、
、![]() 、
、![]() ,设参加反应的四种物质的质量为1,则所消耗氧气的质量分别为1、
,设参加反应的四种物质的质量为1,则所消耗氧气的质量分别为1、![]() 、
、![]() 、
、![]() ,因为
,因为![]() >1>
>1>![]() >
>![]() ,所以消耗氧气的质量由小到大的排列序为③ ④ ① ② 。
,所以消耗氧气的质量由小到大的排列序为③ ④ ① ② 。

 天天向上口算本系列答案
天天向上口算本系列答案【题目】在研究酸和碱的化学性质时,某小组想证明稀硫酸和氢氧化钠混合后,虽然无明显现象,但确实发生了化学反应。试与他们一起完成实验方案的设计、实施和评价,并得出有关结论。
(1)探究稀硫酸和氢氧化钠溶液的反应:
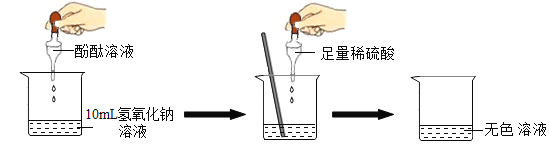
当滴入几滴酚酞溶液后,溶液由无色变为_________色。根据上述实验中颜色变化,可确定稀硫酸和氢氧化钠溶液发生了化学反应。
(2)探究上述稀硫酸和氢氧化钠溶液反应后烧杯中的硫酸是否过量:根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量。同学们又分别选取氯化钡溶液、紫色石蕊溶液设计实验方案,请你判断并(提示:Ba2+与SO42-可形成BaSO4白色沉淀)
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 有白色沉淀生成 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊溶液 | _________ | 稀硫酸过量 |
①上述设计的实验方案中,正确的方案是:__________。
②若请你再设计一个确定稀硫酸是否过量的实验方案,你会选用的药品是_______,实验现象及结论是_____________。
(3)成成同学认为稀硫酸和氢氧化钠溶液的反应没有明显现象,他提出可以对某些有明显现象产生的中和反应进行探究,如稀盐酸和氢氧化铝的反应,可观察到的现象为_________,说明中和反应已经发生,反应的化学方程式为_______________。。(提示:氢氧化铝是不溶于水的白色固体,化学式为Al(OH)3)。
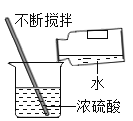
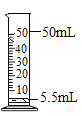
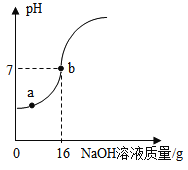
(4)现取10g一定溶质质量分数的稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。计算恰好完全反应时所得溶液的溶质质量分数______。(结果精确到0.1%)
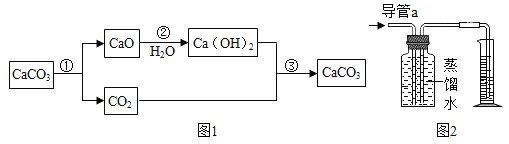
【题目】在化学课上,某活动小组将燃烧的钙迅速伸入到盛满CO2的集气瓶中,钙在其中继续燃烧,反应后冷却,瓶底附着一种白色物质。
(提出问题)小组同学一致认为黑色颗粒是单质碳。那么白色物质是什么呢?
(进行猜想)甲同学认为白色物质是氢氧化钙;乙同学认为白色物质可能是CaO;丙同学认为白色物质是CaCO3;丁同学认为白色物质是______________。其他同学立刻认为甲同学的猜想是错误的,理由是_____________。
(实验探究)
实验方案 | 实验操作 | 实验现象 | 结论 |
方案1 | ①取适量白色物质于试管中,加入适量水,振荡,用手触摸试管外壁。 | __________ | 白色物质中含有CaO。丙同学的猜想不正确 |
②静置后,向上层清液中通入二氧化碳。 | _________ | ||
方案2 | 取样品少量于试管中,加入足量稀盐酸,观察现象。 | 没有气泡产生 |
(实验总结)钙在二氧化碳中燃烧的化学方程式为________________。