题目内容
【题目】通过阅读和观察模型回答问题:
(1)人类发现二氧化碳经历了多个世纪,下列是其历程中的部分资料。
资料一:1630年,海尔蒙特发现在一些洞穴处,有一种能使燃着的蜡烛熄灭的气体,后来被证实是CO2。
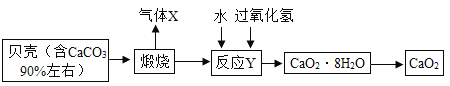
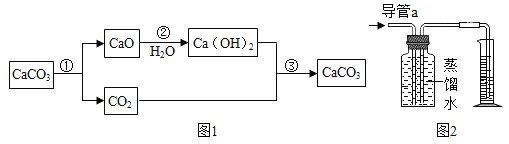
资料二:1754年,布莱克将石灰石煅烧首次制得CO2,并完成如图1所示的物质转化研究。
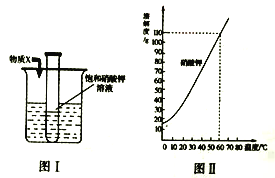
资料三:1766年,卡文迪许通过实验测得:室温下1体积水大约能溶解1体积二氧化碳气体。
①根据海尔蒙特的发现,可推测二氧化碳的化学性质____________。
②写出布莱克实验中既不是化合反应又不是分解反应的一个方程式___________。
③如图2,在室温下将容积为200毫升的广口瓶注满蒸馏水,通过导管a缓慢通入300毫升CO2.如果卡文迪许的结论是正确的,则在量筒中收集到的水约为_______毫升。
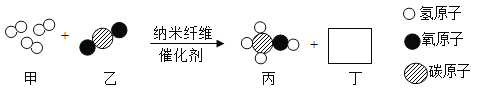
(2)人们常用模型来进行认知,因为这种方式形象直观。图1是水分子和乙炔分子的模型,图2是原子核转变的模型。
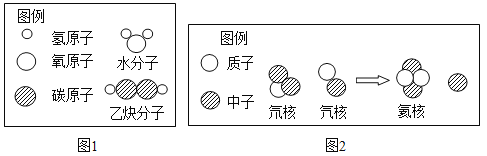
①碳原子和氧原子的画法参照上述图例,请画出“碳和氧气反应生成二氧化碳”的化学反应模型图:________________。
②图1中可作溶剂,对生命活动具有重要作用的物质是___________(写化学式)。乙炔中氢元素的化合价为+1价,请结合模型判断乙炔中碳元素的化合价为______________。
③通过观察氕核和氘核图示,判断氕和氘_________(填是或否)为同种元素,图2是_________(选填“核裂变”或“核聚变”)的示意图。
【答案】不燃烧、也不支持燃烧 Ca(OH)2+CO2= CaCO3↓+H2O 100 ![]() H2O -1 是 核聚变
H2O -1 是 核聚变
【解析】
(1)海尔蒙特的发现: 有一种能使燃着的蜡烛熄灭的气体,说明该气体不燃烧、也不支持燃烧,故填写:不燃烧、也不支持燃烧;
由图可知,碳酸钙一定条件下生成二氧化碳和氧化钙,属于“一变多“的分解反应,氧化钙和水反应生成氢氧化钙,属于“多变一“的化合反应,既不属于化合反应又不属于分解反应的是:氢氧化钙与二氧化碳反应生成沉淀碳酸钙和水,故填写:Ca(OH)2+CO2= CaCO3↓+H2O;
卡文迪认为:室温下1体积水大约能溶解1体积二氧化碳气体,300毫升CO2通入注满蒸馏水的200毫升的广口瓶,其中200毫升CO2会溶于200毫升蒸馏水中,剩余100毫升CO2留在广口瓶中,会使广口瓶内压强增大,为使内外压强相同,将有100毫升蒸馏水流入量筒内,故填写:100;
(2)碳和氧气点燃生成二氧化碳,其中碳是由碳原子构成的,氧气是由氧分子构成的,一个氧分子又由两个氧原子构成,二氧化碳是由二氧化碳分子构成的,一个二氧化碳分子是由两个氧原子和一个碳原子构成,![]() 表示碳原子
表示碳原子![]() 表示氧原子故填写:
表示氧原子故填写: ![]() ;
;
水在人体中含量最多,对生命活动具有重要作用,且可以作溶剂,由图1水分子的微观结构示意图可知,水的化学式为:H2O,故填写:H2O;
由图1乙炔分子的微观结构示意图可知,乙炔的化学式为:C2H2,乙炔中氢元素的化合价为+1价,假设碳元素的化合价为x,根据化合物中,正负化合价代数和为零原则可知,2ⅹ(+1)+2x=0,则x=-1,故填写:-1;
由图2可知,氕核和氘核的质子数都是1,元素种类取决于质子数,因此氕核和氘核属于同种元素,故填写:是;
由图2可知,氕核和氘核变为质子数更大的氦核,属于核聚变,故填写:核聚变。

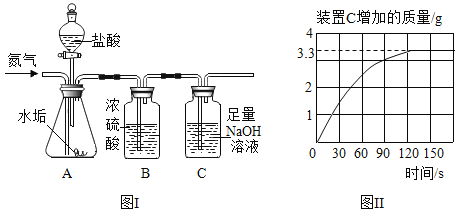
【题目】生铁和钢都是由铁和碳组成的合金,生铁中碳的含量为2%-4.3%,钢中碳的含量为0.03%-2%,为测定某种铁合金中碳的含量,小王同学取一定质量的合金样品盛放在烧杯中,并向其中逐滴加入稀盐酸至恰好完全反应,实验数据如下表所示,注:碳既不溶于水也不与稀盐酸发生反应。
烧杯质量 | 样品的质量 | 稀盐酸的质量 | 烧杯+剩余物的总质量 |
50g | 5.8g | 94.6g | 150.2g |
请根据相关信息完成下列计算:
(1)恰好完全反应时,生成氢气的质量为_________g。
(2)通过计算判断样品是钢还是生铁____________?(计算结果保留到0%)
(3)反应后得到的溶液中溶质的质量分数____________。(计算结果保留到0.1%)