题目内容
【题目】某气体物质3.0g在空气中完全燃烧,生成二氧化碳4.4gCO2,同时生成1.8gH2O.则对该物质相关判断正确的是( )
A. 该物质只含碳、氢元素
B. 该物质由碳、氢、氧元素组成
C. 该物质一定含有碳、氢元素,可能含有氧元素
D. 该物质分子中碳原子和氢原子的个数比为1:2
【答案】BD
【解析】
4.4gCO2中含有碳元素的质量为:4.4g×![]() ×100%=1.2g,1.8g水中含有氢元素的质量为:1.8g×
×100%=1.2g,1.8g水中含有氢元素的质量为:1.8g×![]() ×100%=0.2g,生成物4.4g二氧化碳和1.8g水中所含碳、氢元素的质量和=1.2g+0.2g=1.4g,1.4g<3g,该物质中含氧元素的质量为:3g﹣1.4g=1.6g,则该物质中一定含有碳、氢、氧三种元素。
×100%=0.2g,生成物4.4g二氧化碳和1.8g水中所含碳、氢元素的质量和=1.2g+0.2g=1.4g,1.4g<3g,该物质中含氧元素的质量为:3g﹣1.4g=1.6g,则该物质中一定含有碳、氢、氧三种元素。
A、由上述分析可知,该物质中一定含有碳、氢、氧三种元素,故选项A不正确。
B、由上述分析可知,该物质中一定含有碳、氢、氧三种元素,故选项B正确。
C、由上述分析可知,该物质中一定含有碳、氢、氧三种元素,故选项C不正确。
D、根据化合物原子的个数比=![]() ,则该物质分子中碳原子和氢原子的个数比为
,则该物质分子中碳原子和氢原子的个数比为![]() :
:![]() =1:2,故选项D正确。
=1:2,故选项D正确。
故选:BD。

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案【题目】(探究一)利用如图所示的实验装置制备常见气体,请回答有关问题:
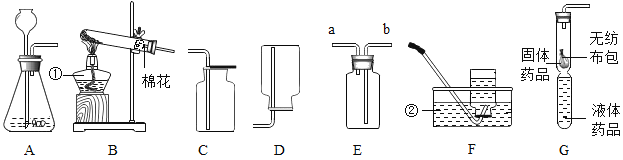
(1)写出标有序号的仪器名称:①_____.②_____.
(2)装置B为气体发生装置,在试管内放入一种暗紫色固体粉末制取氧气以制取氧气,写出有关反应的化学方程式_____.收集装置为_____.
(3)用装置E收集氧气,验满时将带火星的木条放在_____ (选填“a”或“b”)处.
(4)装置G是用软塑料管自制的气体发生装置,利用该装置也可以制取氧气,塑料管中加入的液体药品是_____,药品加入完毕后,要使反应进行,接下来的操作是:_____.
(探究二)探究氧化铁是否像二氧化锰一样可作氯酸钾分解的催化剂同学们设计了三组实验(其他可能影响因素均控制相同):
实验编号 | 实验药品 | 分解温度(℃) |
实验④ | 1.2g KClO3 | T1 |
实验⑤ | 1.2g KClO3、0.5g MnO2 | T2 |
实验⑥ | 1.2g KClO3、0.5g Fe2O3 | T3 |
(1)请写出氯酸钾在二氧化锰催化下制取氧气的化学方程式:_____
(2)若T3_____ (选填“>”、“=”或“<”)T1,说明氧化铁能加快氯酸钾的分解.
(3)若要比较氧化铁与二氧化锰对氯酸钾分解的催化效果,除了可以通过用比较T3与T2的大小,还可以通过排水法收集氧气,测量_____ 进行比较,得出结论.