题目内容
【题目】化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属。流程如下:
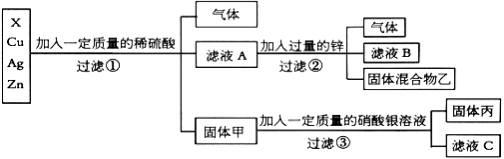
请回答:
(1)四种金属的活动性顺序由强到弱的是 ;
(2)写出步骤②中产生气体的化学方程式 ;
(3)写出步骤③中的反应现象 ;
(4)滤液C中一定含有的溶质是 可能含有的溶质是 ;
【答案】(1)Zn、X、Cu、Ag (2) Zn+H2SO4==ZnSO4+H2↑
(3)溶液有无色逐渐变为蓝色,红色固体逐渐减少 4) Cu(NO3)2 AgNO3
【解析】
试题分析:从图示看出固体甲只有两种金属,说明第一次加入稀硫酸就能反应掉两种金属,由此可以确定金属的活动性为Zn、X、Cu、Ag,最后分离出来的是银,步骤②加入锌可以反应掉过量的硫酸,所以步骤②中产生气体的化学方程式Zn+H2SO4==ZnSO4+H2↑,步骤③的反应就是Cu+2AgNO3=2Ag+C(NO3)2。

练习册系列答案
相关题目