题目内容
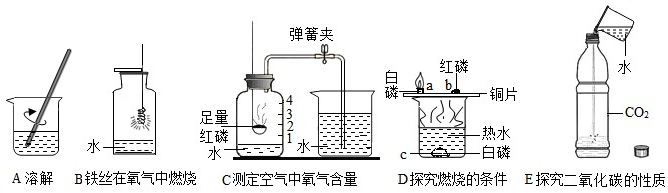
用化学方程式表示实验室制取氧气的反应原理:分析:实验室通常用分解过氧化氢溶液、加热氯酸钾、加热高锰酸钾的方法制取氧气.根据氧气的密度和溶水性来确定收集氧气的方法.
解答:解:实验室制氧气的方法有三种:分解过氧化氢溶液、加热氯酸钾、加热高锰酸钾.氧气的密度比空气大,可用向上排空气法收集,氧气不易溶于水,可用排水法收集.
故答案为:2H2O2
2H2O+O2↑或 2KMnO4
K2 MnO4+MnO2+O2↑或2KClO3
2KCl+3O2↑
向上排空气法或排水法
故答案为:2H2O2
| ||
| ||
| ||||
| △ |
向上排空气法或排水法
点评:收集气体的方法主要有:排水法、向上排空气法、向下排空气法,主要取决于气体的密度、溶水性、是否有毒、是否与水反应、是否与空气中的某物质反应等等.

练习册系列答案
相关题目
某同学在查阅资料时得知:市售纯碱样品常混有氯化钠杂质.
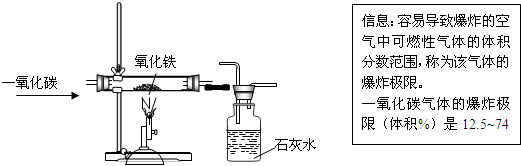
| 资料卡: 侯氏制碱法的原理可以表示为: NaCl+H2O+NH3+CO2 =NaHCO3↓+NH4Cl 2NaHCO3?Na2CO3+CO2 ↑+H2O该同学设计了如图中的装置进行实验,测定市售纯碱样品中碳酸钠的质量分数.(水蒸气的影响忽略不计,夹持装置已略去)  主要实验步骤如下: ①按图组装仪器,并检查装置的气密性; ②称量5.5g市售纯碱样品放入烧瓶中,加适量蒸馏水溶解,得到试样溶液; ③从分液漏斗滴入稀硫酸,直到不再产生气体时为止; ④缓缓鼓入一定量的N2; ⑤称量B瓶及溶液的质量,发现增重2.2g. 请回答下列问题: (1)写出A中发生反应的化学方程式 (2)鼓入一定量的N2的目的是 (3)如果将分液漏斗中的稀硫酸换成浓盐酸,测试的结果(填偏高、偏低或不变) (4)该样品中碳酸钠的质量分数为 (5)若用与上述实验反应原理不同的实验来测定纯碱样品中碳酸钠的质量分数,请用化学方程式表示实验原理 |

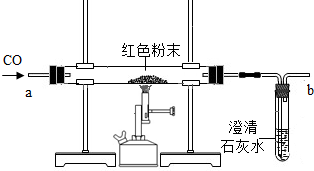 (2007?广元)在实验探究课上,老师给了同学们一包红色粉末,该粉末是铜粉和氧化铁(Fe2O3)粉末中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究活动并回答问题.
(2007?广元)在实验探究课上,老师给了同学们一包红色粉末,该粉末是铜粉和氧化铁(Fe2O3)粉末中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究活动并回答问题.