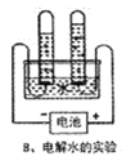
��Ŀ����
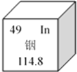
����Ŀ����1���ؿ��е�Ԫ�طֲ���������������ͼ����ش��������⡣

��Ԫ��X��_____����X��Y��ɵĻ�����Ļ�ѧʽ��_____��
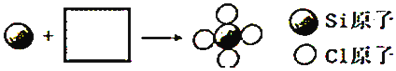
����ͼ��Si��Cl2��Ӧ����SiCl4��ͼʾ�����ں����ϲ�����ȱ��Ӧ���ͼʾ_____��
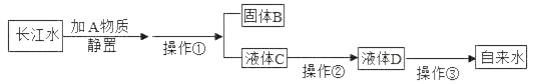
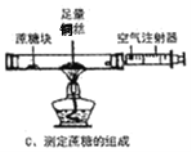
��2���������������ѡ���ʵ���������ա�
a.һ����̼ b.����̿ c.������̼ d.���ʯ e.����
���γ�����ЧӦ��������_____��
�ھ��п�ȼ�Ե����嵥����_____��
���������������_____��
�����ڲò�������_____��
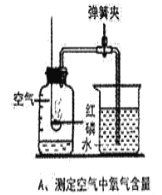
��3����ͼΪľ̿��ԭ����ͭ��װ�ã���ش��������⡣
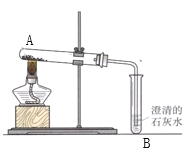
��Ҫ��̼�ۺ�����ͭ��ֻ�Ϻ���װ���Թ��У���������Ŀ�ģ�_____��A�й۲쵽��������_____��
��Ϊ��ʹ����ͭ�е�ͭ��ȫ��Ӧ������������������ͭ��̼�۵������������㽨��ѡ_____����д��ĸ������Ҫ˵���������_____��
A 36��3 B 40:3 C 48:3
���𰸡�O Al2O3  c e a d �����������ĽӴ������ʹ��Ӧ��ֽ��� ��ɫ��ĩ��ɺ�ɫ A ��Ӧ��̿�ۻ����Թ��ڵ�������Ӧ���������ģ����Թ�����̿�������ڷ�Ӧ�Ľ���
c e a d �����������ĽӴ������ʹ��Ӧ��ֽ��� ��ɫ��ĩ��ɺ�ɫ A ��Ӧ��̿�ۻ����Թ��ڵ�������Ӧ���������ģ����Թ�����̿�������ڷ�Ӧ�Ľ���
��������
��1���ٵؿ���Ԫ�صĺ���λ��ǰ��λ��Ԫ������Ϊ�����衢���������ƣ�����X����Ԫ�أ�Y����Ԫ�أ��ڻ������У���Ԫ����+3�ۣ���Ԫ���ԩ�2�ۣ����Զ�����ɵĻ�����Ļ�ѧʽΪAl2O3��
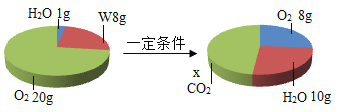
���������غ㶨�ɿ�֪����ѧ��Ӧǰ��ԭ�ӵ���������Ŀ���䣬���Է������������ȷ��ӣ���� ��
��
��2�����γ�����ЧӦ�������Ƕ�����̼������c��
�������Ǿ��п�ȼ�Ե����嵥�ʣ����e��
��һ����̼����������������ж������壬����a��
�ܽ��ʯ��Ӳ���������и��������d��
��3���ٷ�Ӧ��ĽӴ����Խ��ӦԽ��֣���Ҫ��̼�ۺ�����ͭ��ֻ�Ϻ���װ���Թ��У���������Ŀ���ǣ�����ľ̿������ͭ�ĽӴ������ʹ��Ӧ��ֽ��У�����ͭ�ڸ��µ���������̼��Ӧ������ͭ�Ͷ�����̼����A�й۲쵽�������ǣ���ɫ��ĩ��ɺ�ɫ��
����ѡ������ͭ��̼��������ʱҪ�����������ĵ�̼�����ܰ���Ӧ�ı���ѡ��̼��Ӧ�Զ�һЩ�������ڷ�Ӧ�ij�ֽ��С�
![]()

160:12=40:3����̼��Ӧ�Զ�һ�㡣��ѡA�������ǣ���Ӧ��̿�ۻ����Թ��ڵ�������Ӧ���������ģ����Թ�����̿�������ڷ�Ӧ�Ľ��С�