题目内容
【题目】为了测定碳酸钙和氯化钙混合物的组成情况。某学习小组同学取21.lg混合物样品进行了如下图所示的实验:

请回答下列问题:
(1)写出发生反应的化学方程式__________________________________________;
(2)列出求解生成沉淀质量(X)的比例式___________;
(3)混合物样品中碳酸钙与氯化钙的质量比为___________;
(4)C中所得溶液溶质的质量分数为____________;
(5)上述所用的碳酸钠溶液是由26.5%的碳酸钠溶液配制的,需要26.5%的碳酸钠溶液的质量是____________;
【答案】 CaCl2 +Na2CO3===CaCO3 ↓ + 2NaCl 100/106==X/10.6g 或100/106==X/100g× 10.6 g 100:111 10% 40g
【解析】(1).碳酸钙和氯化钙混合物加水溶解后,加入碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;反应方程式为:CaCl2 +Na2CO3===CaCO3 ↓ + 2NaCl;恰好反应时消耗碳酸钠的质量为:100g×10.6%=10.6g,设生成沉淀的质量为x,样品中氯化钙的质量为y,生成氯化钠的质量为m
CaCl2 +Na2CO3===CaCO3 ↓ + 2NaCl
111 106 100 117
y 10.6g x m
106/10.6g=117/m m=11.7g
106/10.6g=100/x 106/10.6g=111/y y=11.1g
样品中碳酸钙的质量为21.1g-11.1g=10g;混合物样品中碳酸钙与氯化钙的质量比为10g:11.1g=100:111;
C中所得溶液溶质的质量分数为11.7g÷(21.1g+100g+100g-20-84.1g)×100%=10%
设需要26.5%的碳酸钠溶液的质量为n 26.5%n=10.6g n=40g
答:略

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。试根据题目要求,回答下列问题(所选仪器装置,填写序号字母):
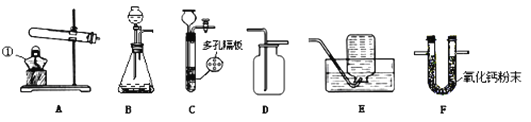
(Ⅰ)写出仪器①的名称:①_____________ 。
(Ⅱ)若用双氧水与二氧化锰为原料制取并收集一瓶干燥的氧气。则应选的气体发生装置为___,反应的化学方程式为______________;应选的气体干燥装置为________。
(Ⅲ)科技小组的同学对实验室制取CO2的实验条件展开了探究,探究实验如下表:
实验编号 | 反应物 | 反应现象 | |
① | 取mg块状大理石 | 足量的溶质质量分数为5%的盐酸 | 产生气泡较慢 |
② | 取mg大理石粉末 | 足量的溶质质量分数为5%的盐酸 | 产生气泡快 |
③ | 取mg块状大理石 | 足量的溶质质量分数为10%的盐酸 | 产生气泡较快 |
④ | 取mg大理石粉末 | 足量的溶质质量分数为10%的盐酸 | 产生气泡很快 |
实验结论:影响大理石和盐酸反应快慢的因素有______ 、________。