题目内容
【题目】水和水溶液是人类必不可少的物质。
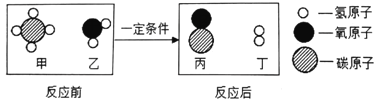
(1)科学家对水的生成和分解实验的研究,确认了水是由______和______组成的。
(2)自然界中的水都不是纯水,利用沉淀、_______、吸附和蒸馏等方法可以净化水。
(3)生活中简便区别硬水和软水的方法是_______________。
(4)下图为甲乙两物质的溶解度曲线。
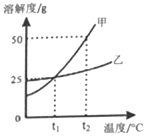
①t2℃时,溶解度较大的物质是_________。
②t1℃时,乙物质饱和溶液中溶质的质量分数为________。
③t2℃时,将50g甲物质放入50g水中,充分溶解后,发现有未溶解的甲物质,其质量是______g。
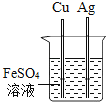
(1)水能灭火,但有时水也能“生火”。比如将过氧化钠(Na2O2)用脱脂棉包裹,再向上面滴加水,脱脂棉一会儿就会发生燃烧。该反应的化学方程式为:2Na2O2+2H2O═4NaOH+X↑。
①X的化学式是______。
②包裹过氧化钠的脱脂棉滴水后,引起脱脂棉能燃烧起来的原因是________。
【答案】 氢元素(或H) 氧元素(或O) 过滤 分别取样,加入肥皂水,搅拌,产生泡沫很少且有白色垢状物形成的水为硬水 甲 20% 25 O2 过氧化钠与水反应放出热量,使脱脂棉的温度达到着火点且产生大量氧气
【解析】(1)物质是由元素组成的,是由科学家对水的生成和分解实验的研究,确认了水是由氢元素和氧元素组成的;
(2)自然界中的水都不是纯水,利用沉淀、过滤、吸附和蒸馏等方法可以净化水;
(3)肥皂水在软水和硬水中的现象不同,所以生活中简便区别硬水和软水的方法是:取样品,加入肥皂水,振荡,产生泡沫较多的是软水,产生泡沫较少的是硬水;
(4)①通过分析溶解度曲线可知,t2℃时,溶解度较大的物质是甲;
②t1℃时,乙物质的溶解度是25g,所以乙物质饱和溶液中溶质的质量分数为![]() ×100%=20%;
×100%=20%;
③t2℃时,甲物质的溶解度是50g,所以将50g甲物质放入50g水中,充分溶解后,发现有未溶解的甲物质,其质量是25g;
(5)①反应物中有4个钠原子,6个氧原子,4个氢原子,生成物中有4个钠原子,4个氢原子,4个氧原子,所以X的化学式是O2;
②燃烧的原因:包括可燃物、温度达到着火点、与氧气接触。过氧化钠与水反应,放出热量,使脱脂棉的温度达到着火点。而且产生大量氧气。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案【题目】兴趣小组同学为了探究实验室中久置的氢氧化纳固体的成分,进行了有关实验。
(1)(对固体猜想)
猜想一:全部是NaOH;猜想二:全部是Na2CO3;猜想三:是NaOH和Na2CO3混合物
(2)(实验和推断)为进一步确定成分,进行了以下探究:
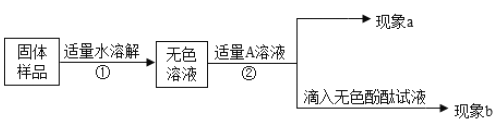
对无色溶液进行以下实验:
实验操作 | 实验现象 | 实验结论 |
第一步: 用试管取约2mL该溶液,滴入适量氢氧化钙溶液,振荡。 | 现象a:白色沉淀 | 化学方程式: ①____________________, 有碳酸钠并全部除尽。 |
第二步: 静置,取上层清液于试管中滴入酚酞溶液,振荡。 | 现象b: ②____________________ | 含有NaOH,猜想三成立,是NaOH和Na2CO3混合物 |
③小组中有同学提出质疑,认为以上实验不能证明猜想三成立,理由是:______。
④反思:把第一步中的氢氧化钙溶液换成__________溶液,可达到实验目的。
(3)请利用以下提供的试剂(提供的试剂有:酚酞溶液、稀盐酸、氢氧化钡溶液、氯化钡溶液),设计实验证明猜想一(即氢氧化钠没有变质)是正确的。您设计的实验方案:__________________。