题目内容
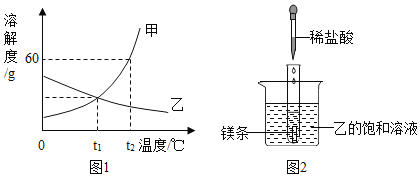
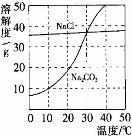
【题目】图为氯化钠、碳酸钠在水中的溶解度曲线。
请回答下列问题:
(1)10℃时,碳酸钠的溶解度为 g;
(2)30℃时,氯化钠的溶解度 碳酸钠的溶解度(填写“>”、“<”或“=”);
(3)10℃时,向两只盛有100g水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质是 ,其中 (填溶质)质量较大。
(4)将碳酸钠不饱和溶液转化为饱和溶液的方法有 、 (至少填两种)。
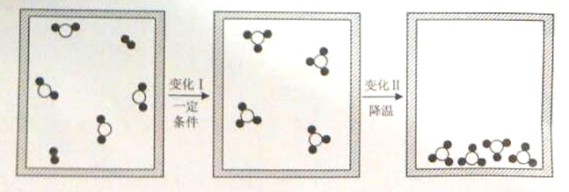
(5)如图所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是________(填字母序号)
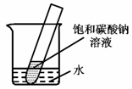
A.氢氧化钠 B.氯化钠 C.硝酸铵
【答案】(1)10
(2)=
(3)氯化钠、碳酸钠; 氯化钠
(4)加碳酸钠、蒸发水、降温
(5)C
【解析】(1)根据溶解度曲线的意义解答;
(2)根据曲线中交点的含义考虑;
(3)关键要根据该温度时的溶解度看所加物质是否全部溶解;
(4)根据饱和溶液与不饱和溶液之间的转化方法解答;
(5)物质溶于水吸热和放热情况考虑.
解答:解:(1)10℃时,碳酸钠的溶解度为10g;
(2)曲线中交点表示该温度时两种物质的溶解度相等,所以30℃时氯化钠和碳酸钠两物质的溶解度相等;
(3)10℃时,碳酸钠的溶解度为10g,氯化钠的溶解度大于碳酸钠,所以所得溶液中食盐的质量多.
(3)碳酸钠的溶解度随温度升高而增大,将碳酸钠不饱和溶液转化为饱和溶液的方法有加碳酸钠,蒸发水、降温.
(4)由饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出,说明温度降低了,也就是说该物质溶于水是吸热的,所以为硝酸铵.
故答案为:
(1)10g;
(2)═;
(3)氯化钠、碳酸钠;氯化钠;
(4)>;
(4)加碳酸钠,蒸发水、降温;
(5)C.

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案【题目】煅烧石灰石(主要成分 CaCO3)生成生石灰(CaO)和二氧化碳。为了测定某石灰石中碳酸钙(CaCO3)的含量,现称取 24.0g 石灰石样品,进行四次高温煅烧、冷却,称量剩余固体的质量 (杂质不参加反应),记录实验数据如下:
操作 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量 | 21.6g | 19.2g | 15.2g | 15.2g |
试计算:
(1)完全反应后生成二氧化碳的质量为_____;
(2)求该石灰石样品中碳酸钙的质量_____。