题目内容
【题目】KCl和KNO3的溶解度表及溶解度曲线如下图所示,下列说法不正确的是 ( )

A. 甲表示KCl溶解度曲线
B. 两物质溶解度相等的温度t1在20℃~30℃
C. 40℃时,5gKCl加入10g水中,可得到33.3%的溶液
D. 50℃时,30g KNO3加入50g水,充分溶解,再降温到30℃,有晶体析出
【答案】AC
【解析】根据已有溶解度的意义结合题干提供的信息进行分析解答即可,溶质质量分数就是溶质质量与溶液质量的比值,据此解答。
解:A、由图示结合表格可知,甲的溶解度受温度的影响变化较大,应表示KNO3溶解度曲线,故错误;
B、根据表格可以看出,KCl与KNO3两物质的溶解度相等的温度在20﹣30℃之间,正确;
C、在40℃时,KCl的溶解度为40g,10g水中最多溶解4g,溶液的最大浓度可达到![]() ,不是33.3%,错误;
,不是33.3%,错误;
D、在50℃时,硝酸钾的溶解度为85.5g,40℃时,硝酸钾的溶解度为45.8g,在50℃时,将10g KNO3中加20g水,全部溶解,在30℃时,20g水中最多溶解
9.16g,故再降温到30℃,有KNO3固体析出,正确。
故选A 、C。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下:
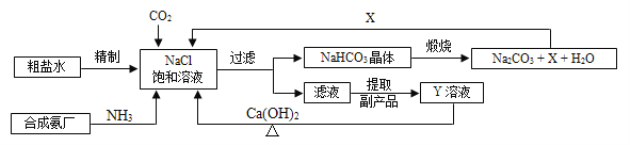
(1)粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的① NaOH溶液、② Na2CO3溶液、③ BaCl2溶液及适量的盐酸等除杂、精制。则加入试剂合理的顺序为_____________(填字母序号)。
A.①②③ B.③②① C.①③②
(2)加盐酸的作用是(用方程式表示)________________、______________。
(3)制碱原理可看作是由① CO2 + NH3 + H2O = NH4HCO3和② NaCl + NH4HCO3 = NaHCO3+ NH4Cl两个反应加合而成。反应②为复分解反应,请根据复分解反应发生的条件及表1中相关物质20℃时的溶解度,分析反应②为何能顺利进行?_______________。
表1 相关物质的溶解度(20℃)(单位:g)
NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
36.0 | 21.7 | 9.6 | 37.2 |
(4)操作2为洗涤、煅烧。晶体应在以下装置______________中(填字母序号)进行“洗涤”操作。

在上述操作中,如何判断晶体已经洗涤干净______________。
(5)X的化学式为_____________,若X直接排放到空气中会造成的后果是_______________。
(6)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为______________,Y的化学式为______________,写出Y的一种用途_____________。